Панкреатическая рибонуклеаза
Cтраница 3
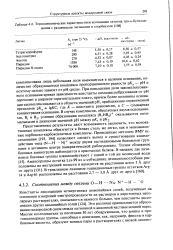 |
Термодинамические характеристики ассоциации катиона три-н-бутилам-мония с различными лигандами в хлорбензоле. [31] |
Представленные результаты дают возможность заключить, что монока-тионные комплексы образуются в белках столь же легко, как и моноанионные карбоксил-карбоксилатные комплексы. Проведенные методом ЯМР исследования [193, 194] позволяют сделать вывод о существовании взаимодействия типа ( N - Н N) между двумя гистидиновыми боковыми группами в активном центре панкреатической рибонуклеазы. Тесное сближение боковых аминогрупп наблюдается в кристаллах белков. [32]
Значительную ценность представляют собой рибонуклеазы высокой специфичности, так как они не только расщепляют нуклеиновую кислоту на олигонуклеотиды, которые во многих случаях можно разделить и определить их структуру, но и указывают также в общем распределение нуклеотидов. Так, обнаружено, что пропорция пиримидиновых нуклеозид-3 - фосфатов ( по отношению к общему содержанию пиримидинов в нуклеиновой кислоте), выде ляющихся под действием панкреатической рибонуклеазы, в значительной степени варьирует. При известной специфичности фермента высокий процент выделения свободных пиримидиновых нуклеотидов по отношению к общему содержанию пиримидинов указывает на наличие участков цепи, в которых два или более пиримидинов следуют подряд друг за другом, в то время как выделение моно-нуклеотидов в относительно малом количестве указывает на то, что пиримидиновые нуклеотиды в основном соединены ( через 5 -гидро-ксильную группу) с З - фосфатами пуриновых нуклеотидных звеньев. Из рибонуклеиновой кислоты вируса табачной мозаики штамма М после исчерпывающего переваривания панкреатической рибонуклеазой выделено значительно большее количество пиримидиновых нуклеотидов, чем в случае штаммов TMV, HR и YA; следовательно, распределение пиримидиновых нуклеотидов в РНК из штамма М отличается от распределения нуклеотидов в РНК штаммов TMV, HR или YA [162] ( ср. [33]
Связываясь с матричным полинуклеотидом и удерживая его в ходе трансляции, рибосома защищает от действия внешних нуклеаз довольно протяженный участок цепи. Еще в ранних опытах с поли ( 1 Г) было показано, что рибосома покрывает участок длиной около 25 нуклеотидных остатков, делая его недоступным для панкреатической рибонуклеазы. В последних опытах было показано, что функциональная 70S рибосома, несущая тРНК, защищает от нуклеаз участок матричного полинуклеотида длиной около 45 - 50 нуклеотидных остатков, причем в пределах защищаемого участка имеется относительно доступная точка, разрыв при которой дает фрагменты длиной 27 - 30 остатков и около 15 - 20 остатков. Из некоторых наблюдений следует, что эта чувствительная точка матрицы находится непосредственно перед кодоном, связанным с тРНК в А-участке рибосомы; защищаемый 15-нуклеотидный фрагмент представляет собой 3 -проксимальную часть, а 30-нуклеотидный фрагмент-5 - проксималь-ную часть связанного рибосомой участка матрицы. [34]
Хотя на данном этапе методы химического гидролиза не позволяют сделать выбора между 3 - 5 - и 2 - 5 -межнуклеотидными связями, доказательства, по-видимому, исключительного присутствия 3 - 5 -структуры были получены на основании исследований ферментативного гидролиза рибонуклеиновых кислот и простых нуклеотидных производных. Из различных источников был выделен ряд нуклеаз, которые катализируют гидролиз нуклеиновых кислот на более мелкие фрагменты. Панкреатическая рибонуклеаза [93] - один из группы ферментов, обнаруживающих высокую специфичность к рибонуклеиновым кислотам - была тщательно изучена и дано объяснение механизма ее действия. [35]
Недавно исследованы рибонуклеазы, имеющие даже большую специфичность, чем основной компонент кристаллического фермента из поджелудочной железы. Конечным продуктом гидролиза дрожжевой рибонуклеиновой кислоты является гуанозин-3 - фосфат ( около 40 % общего содержания гуанина) и олигонуклеотиды с гуанозин-3 - фосфатом на конце. Как и в случае панкреатической рибонуклеазы, стадия трансфосфорилирования обратима [169, 170] и фермент катализирует как полимеризацию гуанозин-2 3 -циклофосфата до олиго-и, возможно, полигуаниловой кислот, так и трансфосфорилирова-ние 5 -гидроксильной группы нуклеозидов ( с образованием дину-клеозидфосфатов, таких, как гуанилил-3: 5 -уридин и гуанилил-3: 5 -аденозин), нуклеозид - З - фосфатов и нуклеозид-2 3 -цикло-фосфатов. [36]
Субстратная специфичность заключается в доступности точек контакта в белке для пиримидиновых или пуриновых оснований; специфическое действие ( расщепление связи 3 - О - Р или 5 - О - - Р) состоит не во внутримолекулярном образовании водородных связей в субстрате, а в нуклеофильной атаке на определенную сторону атома фосфора ( определяемую конформацией фермента и расположением точки контакта воды), обеспечивающей вытеснение определенной группы с противоположной стороны. На схемах специфичность субстрата указывается наклоном контуров фермента. Общая схема предполагает, что панкреатическая рибонуклеаза может обладать очень низкой активностью по отношению к пурино-вым производным. [37]
После высушивания пластинки промывают водой и вновь высушивают. Продукты гидролиза РНК, полученные при обработке ее панкреатической рибонуклеазой или смесью панкреатической рибонуклеазы и рибонуклеазы Т ], наносят на расстоянии 5 см от одного из краев пластинки двумя порциями по 1 мкл, содержащими 2 - 3 ЕПаео ( см. статью Тенера, стр. [38]
После высушивания пластинки промывают водой и вновь высушивают. Продукты гидролиза РНК, полученные при обработке ее панкреатической рибонуклеазой или смесью панкреатической рибонуклеазы и рибонуклеазы Т ], наносят на расстоянии 5 см от одного из краев пластинки двумя порциями по 1 мкл, содержащими 2 - 3 ЕПаео ( см. статью Тенера, стр. [39]
С помощью химического и ферментативного гидролиза было показано, что синтетические полинуклеотиды, как и РНК, состоят из нуклеозид-5 - монофосфатных единиц, связанных между собой 3 5 -фосфодиэфирными связями ( стр. Анализ концевых групп показал, что на конце полипептидной цепи находится фосфатная группа, этерифицированная по С-5 концевого нуклеозида. При гидролизе щелочью, фосфодиэстеразой змеиного яда, фосфо-диэстеразой из селезенки или панкреатической рибонуклеазой эти полимеры дают точно такие же продукты, как и РНК. [40]
В блочном методе определения последовательности нуклеиновых кислот весьма существенна методология структурного анализа. В одном из возможных вариантов используется полное расщепление полинуклеотидной цепи двумя ( или более) ферментами с различной специфичностью. В случае РНК это может быть осуществлено различными рибонуклеаза ми, например гидролиз последовательно рибонуклеазой Ти а затем - панкреатической рибонуклеазой. Структуры полученных олигонуклеотидов сравниваются для поиска перекрывающихся последовательностей. Если это оказывается недостаточным, используется третья РНаза. [41]
Получают как промежуточное соединение при гидрол. Легко превращается в З - фосфат нуклеазой Т, и рибонуклеазой из листьев растений и в смесь 2 - и З - фосфатов разб. Не атакуется панкреатической рибонуклеазой. [42]
Значительную ценность представляют собой рибонуклеазы высокой специфичности, так как они не только расщепляют нуклеиновую кислоту на олигонуклеотиды, которые во многих случаях можно разделить и определить их структуру, но и указывают также в общем распределение нуклеотидов. Так, обнаружено, что пропорция пиримидиновых нуклеозид-3 - фосфатов ( по отношению к общему содержанию пиримидинов в нуклеиновой кислоте), выде ляющихся под действием панкреатической рибонуклеазы, в значительной степени варьирует. При известной специфичности фермента высокий процент выделения свободных пиримидиновых нуклеотидов по отношению к общему содержанию пиримидинов указывает на наличие участков цепи, в которых два или более пиримидинов следуют подряд друг за другом, в то время как выделение моно-нуклеотидов в относительно малом количестве указывает на то, что пиримидиновые нуклеотиды в основном соединены ( через 5 -гидро-ксильную группу) с З - фосфатами пуриновых нуклеотидных звеньев. Из рибонуклеиновой кислоты вируса табачной мозаики штамма М после исчерпывающего переваривания панкреатической рибонуклеазой выделено значительно большее количество пиримидиновых нуклеотидов, чем в случае штаммов TMV, HR и YA; следовательно, распределение пиримидиновых нуклеотидов в РНК из штамма М отличается от распределения нуклеотидов в РНК штаммов TMV, HR или YA [162] ( ср. [43]
Первая группа - близкие аналоги субстратов, содержащие весь набор или, по крайней мере, большую часть групп, узнаваемых активным центром фермента, и поэтому образующие комплекс фермент - аналог, сходный с комплексом фермент - субстрат. Однако в силу специфики своей структуры они не подвергаются ферментативному превращению. Занимая активный центр, эти аналоги препятствуют связыванию субстрата и тем самым ферментативной реакции. Например, соединение ( 95) имеет весь набор групп, узнаваемых панкреатической рибонуклеазой ( см. рис. 59, 60), но CJb-группа, стоящая вместо атома 5 - 0 субстрата, не способна принять протон от протонированного His-119 и расщепления связи Р - - С не происходит. Фенилпропионовая кислота содержит карбоксильную группу и гидрофобный фенильный радикал, в связи с чем связывается с активным центром карбокси пептид азы А ( см. рис. 62), но не имеет амидпой группировки и никакому превращению ферментом поэтому не подвергается. Оба указанных соединения являются типичными конкурентными ингибиторами соответственно панкреатической рибонуклеазы и карбоксипептидазы А. [44]
Для исследования нуклеотидных последовательностей акцепторного конца т - РНК в лаборатории Д. Г. Кнорре был применен кинетический подход. Для установления полной структуры молекулы т - РНК в этой же лаборатории С. К. Василенко был предложен очень интересный и перспективный метод. Для индивидуальной т - РНК составляется карта олигонуклеотидов, образующихся при полном ферментативном гидролизе таких т - РНК или панкреатической рибонуклеазой или гуанилрибонуклеазой. Для каждой фракции переваренной РНК составляется аналогичная олигонуклеотидная карта. Исчезновение определенных олигонуклеотидов в исходной карте делает возможным установить местоположение этих олигонуклеотидов в полинуклеотидной цепи исходной молекулы т - РНК. [45]
Страницы: 1 2 3 4