Рибофлавин
Cтраница 2
Рибофлавин широко распространен в природе - в микроорганизмах, в растительных и животных клетках, однако животные организмы не способны к самостоятельному биосинтезу рибофлавина и получают его или с пищей, или в результате деятельности микрофлоры желудочно-кишечного тракта. В виде соединения с фосфорной кислотой ( рибофлавин-5 - фосфат, ФМН), или соединения ФМН с АМФ ( флавинадениндинуклеотид, ФАД), или 8 а-производных ФАД, ковалентно связанных с белком, которые в свою очередь связываются с апоферментами и обычно с металлами ( флавиновые ферменты), рибофлавин находится в различных органах и тканях [308], почти во всех аэробных клетках. Однако в животных тканях рибофлавин находится преимущественно в виде ФМН, ФАД и 8 а-производных ФАД. В тканях человеческого организма содержится около 85 % ФАД, от 10 до 15 % ФМН и только несколько - процентов рибофлавина. [16]
Рибофлавин обычно накапливается в сетчатке глаза у позвоночных. Хорошим примером тому служат такие животные, как галаго ( Galago), у которого золотисто-желтые кристаллы рибофлавина составляют прозрачный отражающий слой, выстилающий сзади сетчатку. В глазах членистоногих рибофлавин в отличие от птеринов не обнаружен. [17]
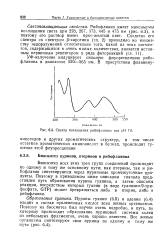 |
Спектр поглощения рибофлавина при рН. [18] |
Рибофлавин имеет максимумы поглощения света при 223, 267, 373, 445 и 475 нм ( рис. 6.3), и поэтому его раствор имеет ярко-желтый цвет. [19]
Рибофлавин, связанный с фосфорной кислотой, входит в состав ферментов, обычно называемых флавиновыми ферментами. Желтый рибофлавин сообщает желтую окраску флавиновым ферментам, входящим в группу аэробных дегидрогеназ. Таким образом, витамин В2 участвует в окислительно-восстановительных процессах. Рибофлавин встречается в виде флавинмононуклеотида ( ФМН) и флавинадениндинуклеотида ( ФАД), а также в связанном с белками состоянии, образуя качественно новые системы - желтые дыхательные ферменты. Нейтральный водный раствор рибофлавина обладает желто-зеленой флуоресценцией. При подкислении или при подщелачивании флуоресценция рибофлавина уменьшается и исчезает. В щелочной среде витамин В2 разрушается, в кислой среде он устойчив. [20]
 |
Содержание витамина В2 в пищевых продуктах. [21] |
Рибофлавин кристаллизуется в виде игл желтого цвета с температурой плавления 290 С. В отличие от витамина Bj рибофлавин более термостабилен, вместе с тем он весьма чувствителен к свету, под действием которого возможен его распад. Источником витамина В2 являются растительные и микробные клетки. Животный организм не способен к синтезу рибофлавина и получает его или с пищей, или в результате синтеза кишечной микрофлорой. [22]
Рибофлавин следует хранить в сухом и темном месте. [23]
Рибофлавин широко распространен в природе. Из продуктов питания наиболее богаты им мясо, печень, дрожжи, яйца, томаты. [24]
Рибофлавин трудно растворим в воде. [25]
Рибофлавин в больших концентрациях и в растворах с низким значением рН более устойчив к действию света, чем при низких концентрациях в щелочных условиях. Аскорбиновая кислота, чайный танин способны замедлять разрушение рибофлавина. Рибофлавин устойчив к кислотам, брому и к таким окислителям, как перекись водорода и концентрированная азотная кислота. [26]
Рибофлавин ( витамин В2) является фактором нормального роста животных организмов. [27]
Рибофлавин обладает окислительно-восстановительными свойствами. Физиологическая роль витамина Вй выяснилась, когда было установлено, что рибофлавин входит в состав коферментов ФАД и ФМН, являющихся простетической группой ряда ферментов, относящихся к классу оксидоредуктаз. [28]
Рибофлавин входит в молекулу фермента в виде соединения с фосфорной, адениловой кислотами в виде кофермента. [29]
Рибофлавин входит в состав простетической группы ферментов только в виде фосфорных эфиров. [30]
Страницы: 1 2 3 4