Абсолютное значение - скорость - реакция
Cтраница 1
Абсолютные значения скоростей реакции при сохранении указанной зависимости могут изменяться в широких пределах, в соответствии с изменением основных факторов окисления. [1]
 |
Зависимость скорости реакции от. [2] |
Абсолютные значения скорости реакции оказались на несколько порядков выше, чем в обработанных сосудах. [3]
Абсолютные значения скоростей реакций могут различаться очень сильно, в соответствии с ними выбирают технологические параметры установок для обезвреживания газовых сред. [4]
 |
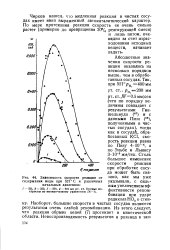
Интегральные кривые уравнения теп - уП лопроводности в пламени ( римские цифры - номера горючих систем. [5] |
Абсолютные значения скорости реакции в пламени [12, 61], При разработках теории горения и ее технических приложений обычно определяют зависимость скорости пламени и скорости реакции в пламени от основных варьируемых параметров - температуры, давления и состава. Однако такие сведения не всегда достаточны, оказывается желательным оценить также абсолютные значения скорости реакции в пламени и возможность дальнейшей интенсификации процесса горения. Уравнение (3.76) позволяет вычислить максимальное значение скорости реакции в пламени Фтах. [6]
 |
Типичные кривые тепловыделения. [7] |
Абсолютное значение скорости реакции зависит от концентрации пересыщения, толщины диффузионных слоев на растворяющихся зернах, констант скорости растворения и роста кристаллов и многих других факторов. [8]
Для абсолютных значений скорости реакции такое согласие теоретических и экспериментальных значений вполне удовлетворительно, поскольку значения kl ненадежны. [9]
Определение абсолютных значений скорости реакции не дает прямых сведений о кинетических закономерностях, однако иногда дает возможность скорее обнаружить ошибку и измерений. Особенности кинетики реакции в пламени, обусловленные ее цепным механизмом, могут приводить к нарушениям описанных закономерностей нормального горения. [10]
Более того, абсолютное значение скорости реакции с участием иона С1 - становится в диметилформамиде в 1 3 - 10е раз больше, чем в воде. Еще более сильное влияние растворителя на скорость реакции было обнаружено в катализируемом метоксильными ионами процессе обмена протонов, расположенных в молекуле рядом с активирующей циано-группой, сложно-эфирной или амидной группой. [11]
Предпринято несколько попыток определить точные абсолютные значения скоростей реакций метилена. Так, при помощи ряда изящных экспериментов, заключающихся в одновременном импульсном фотолизе смесей кетена с инертным газом и кетена с этиленом, Кистяковскому и Зауэру [1 ] удалось показать, что метилен реагирует с кетеном по меньшей мере при одном из каждых 200 соударений. [12]
 |
& Независимость скорости ( и взаимодействия Н2О и С от давления Р паров воды при 2450 К. [13] |
Значительные расхождения данных по абсолютным значениям скоростей реакции объясняются, по-видимому, так же, как. [14]
 |
Относительные скорости реакции фенола с формальдегидом. [15] |
Страницы: 1 2 3