Рост - потенциал
Cтраница 2
В действительности рост потенциала не может продолжаться безгранично. При достаточном смещении потенциала в сторону отрицательных значений начнется процесс выделения водорода, который будет наложен на кислородную деполяризацию. [16]
В действительности рост потенциалов не может продолжаться безгранично, так как при достаточном смещении потенциала катода в отрицательную сторону на электроде, помимо ионизации кислорода, может начаться какой-либо новый электродный процесс. В водных растворах таким процессом обычно оказывается катодное выделение водорода с потенциала на 1 23 В отрицательнее равновесного потенциала ионизации кислорода. [17]
В действительности рост потенциалов не продолжается безгранично, так как при достижении определенного потенциала помимо ионизации кислорода начинается процесс выделения водорода. [18]
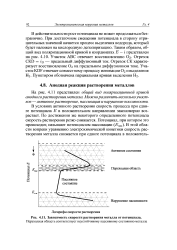 |
Зависимость скорости растворения металла от потенциала. [19] |
В действительности рост потенциала не может продолжаться безгранично. При достаточном смещении потенциала в сторону отрицательных значений начнется процесс выделения водорода, который будет наложен на кислородную деполяризацию. [20]
В результате роста потенциала становится возможным раз - ряд ионов гидроксила, и получающиеся при этом радикалы ОН, а может быть и атомарный кислород, реагируя с металлом, образуют окиси, которые в виде тонкой, хорошо пристающей и невидимой пленки осаждаются под толстым видимым, но не плотно прилегающим слоем соли. Пленка окиси быстро распространяется по поверхности анода и, когда вся поверхность оказывается закрытой ею, начинается выделение кислорода. [21]
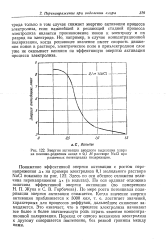 |
Энергия активации анодного выделения хлора. [22] |
По мере роста потенциала поляризации энергия активации снижается. Это означает, что в процессе электролиза начинают все более и более значительную роль играть явления концентрационной поляризации. Переход от одного механизма электролиза к другому совершается постепенно, без резкой границы между ними. [23]
Поэтому с ростом потенциала выход по току на растворение Ru снижается. [24]
С этого момента рост потенциала электрода как бы отстает от роста налагаемого внешнего напряжения - электрод деполяризуется. Вещество, участвующее в электрохимической реакции и вызывающее деполяризацию электрода, называют деполяризатором. На этом участке сила тока практически не зависит от потенциала электрода. В результате обеднения приэлектродного слоя по сравнению с объемом раствора, где концентрация кадмия ( II) равна исходной величине, возникает градиент концентраций, вызывающий диффузию ионов кадмия ( II) в обедненный слой. Диффундирующие к поверхности электрода ионы кадмия ( II) восстанавливаются, а поскольку разность концентраций между электродным слоем и объемом раствора за счет протекания ничтожно малых ( микроамперных) токов практически не меняется, предельный ток на участке ВГ остается постоянным. Он остается постоянным до потенциала, когда на электроде начинается новая электрохимическая реакция ( восстановление другого деполяризатора или разряд катиона фонового электролита) и наблюдается новый подъем тока. Ток, обусловленный электрохимической реакцией на электроде, называют фарадеевским, подчеркивая его связь с процессом электролиза. [25]
Высказано предположение, что рост потенциала связан с осаждением на поверхности катода примесей в электролите, про-мотирующих внедрение атомов водорода в металл и приводящих к повышению концентрации адсорбированного водорода. [26]
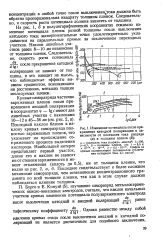 |
Изменение потенциала после прекращения катодной поляризации в зависимости от плотности тока разряда ( а и толщины пленок ( б. [27] |
Следовательно, и скорость роста потенциала должна зависеть от толщины. [28]
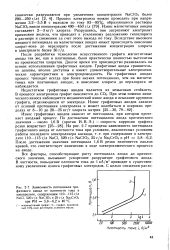 |
Зависимость потенциала графитового анода от плотности тока в электролите, содержащем ПО-115 г / л NaCl, 520 г / л NaCiCb и 25 г / л Na2CrO4 при РН 5 8 - 6 2 и 40 С. [29] |
Все факторы, способствующие росту потенциала анода до критического значения, вызывают ускоренное разрушение графитового анода. В частности, повышение плотности тока до 1 кА / м2 приводит к существенному увеличению износа графитовых электродов. [30]
Страницы: 1 2 3 4