Рост - потенциал
Cтраница 4
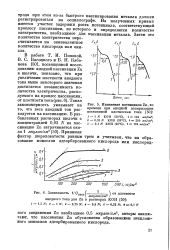 |
Изменение потенциала Zn, во времени при анодной поляризации постоянной плотностью тока. [46] |
На полученных кривых имеется участок задержки роста потенциала, соответствующий процессу пассивации, из которого и определяется количество электричества, необходимое для пассивации металла. Затем это количество электричества пере-считывается на эквивалентное количество кислорода или окисла. [47]
В связи с этим по мере роста потенциала ионизации газа столба увеличиваются температура Тн и разность АГ Тн - Тк, поскольку температура активного пятна ограничена температурой кипения катода Тк и остается постоянной. В соответствии с уравнением ( 2 - 9) это приводит, при прочих равных условиях, к увеличению напряжения катодной области. [48]
Увеличение тока / к0 приведет к росту потенциала эмиттера и, соответственно, на базе транзистора, поскольку разность потенциалов эмиттер - база близка к нулю. Это приводит к уменьшению тока через резистор Ra и к возрастанию тока через резистор R Ток / б, равный разности этих токов, уменьшается. [49]
Энергия активации электрохимической реакции понижается с ростом потенциала поляризации. Полученный результат также можно считать физически вполне естественным. [50]
Стабильность поверхностных я-комплексов должна снижаться с ростом потенциала ионизации - как это имеет место в случае я-комплексов в объеме. Однако в докладе делается исключение из такого правила для алкилбензолов. Авторы утверждают, что метильные группы на поверхности создают стерические затруднения, причем этот эффект перекрывает электронные эффекты, обусловленные изменением ионизационного потенциала, так что ряды стабильности для поверхностных и объемных комплексов будут противоположными. [51]
 |
Зависимость Е от значения х, и х2 для реакций окисления и восстановления оксидов железа. [52] |
Как видно из рисунка 29, с ростом потенциала становятся более вероятными области существования высших оксидов железа. [53]
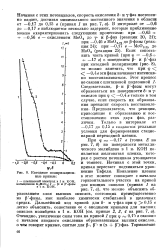 |
Катодные поляризационные кривые. [54] |
КОН появляется желтоватая пленка, которая с ростом потенциала утолщается и темнеет. Начиная с этой точки, кривая перестает подчиняться уравнению Тафеля. Появление пленки в этот момент совпадает с началом горизонтального участка на кривой для низших окислов ( кривая 1 на рис. 7, а), что можно объяснить образованием слоя высших окислов, состоящих преимущественно из р - фазы, как наиболее химически стабильной в щелочных средах. Очевидно, увеличение силы тока на кривой 1 при ф 0 15 в связано с началом анодного окисления образовавшихся высших окислов, о чем говорят кривые, снятые для Р -, Р - и ( а р) - фаз. [55]
Это связано, прежде всего, с ростом потенциалов ионизации Sd-электронов. Уменьшение этого расстояния связано также с тем фактом, что Зй. Z становится все более локализованным и теряет свой валентный характер. [56]
 |
Элекрокапиллярная кривая. [57] |
С этого момента рост тока как бы опережает рост потенциала электрода - электрод деполяризуется. [58]
Замещение водорода, имино-группы на метиль-ную группу вызывает рост потенциала окисления, чего не наблюдается для других аминов. Введение же метальных групп в кольца приводит, как и ожидалось, к понижению потенциала окисления. В этом случае кислота, по-видимому, нейтрализует и делает неактивной алифатическую амино-группу боковой цепи. [59]
Страницы: 1 2 3 4