Рассчитанное значение - энергия
Cтраница 2
В зависимости от вида дооавки принципиально различается характер взаимодействия их о Дисперсионной средой, на что указывают рассчитанные значения энергии активации вязкого течения. [16]
В ультрафиолетовой спектроскопии в качестве меры положения полосы используют как длины волн, так и волновые числа, которые, будучи пропорциональными энергетическим величинам, легче сопоставляются с рассчитанными значениями энергии перехода. При переводе длин волн, в которых проградуированы шкалы большинства промышленных спектрофотометров, в волновые числа следует учитывать погрешность их определения, которая для СФ-16 составляет 1 нм. [17]
 |
Устойчивость металлокарбоангидраз. [18] |
Температурная зависимость этого процесса удовлетворительно выражается кривой Аррениуса. Рассчитанные значения энергии и энтропии активации приведены в табл. 16.10. Наблюдаемые величины энергии активации выше энергий активации модельных систем, но частично компенсируются большим выигрышем в энтропии активации. [19]
Второй подход использует теорему Купменса, утверждающую примерное равенство орбитальной энергии и энергии связи Есъ электрона. В то же время рассчитанные значения энергии обычно плохо согласуются с большими абсолютными значениями Есв. [20]
В табл. 2.4 также приведены некоторые рассчитанные значения энергий ароматизации, которые представляют собой разницу энергий аналогов с локализованными и делокализованными структурами. [21]
Для несимметричных молекул величина С приобретает иной вид и зависит от длины молекул и их взаимной ориентации. Формула (III.1) перестает быть верной при увеличении молекулярного веса взаимодействующих молекул, при этом рассчитанное значение энергии дисперсионных сил оказывается завышенным. [22]
Порядок величины энергии активации, связанной с вязкостью, был оценен, исходя из предположения, что движущаяся группа окружена пустотами, объем которых больше некоторого критического значения. Критический объем рассчитывается, исходя из потенциала межмолекулярного взаимодействия в форме Леннарда - Джонса. Рассчитанное значение энергии активации для процесса локальных колебаний составляет около 42 кДж / моль. [23]
Для выяснения фактора, лимитирующего образование склонности к МКК, определены энергии активации диффузионных процессов для стали в закаленном состоянии и после МТО с последеформационным нагревом при 600 С. Расчет энергии активации диффузионных процессов Q ( по наклону прямых 1 и 2, рис. 1) дал значение 43 - 45 ккал / г-атом ( для закаленной стали) и близкую по своему значению величину энергии 40 - 42 ккал / г-атом для стали, подвергнутой механико-термической обработке. Из рассчитанных значений энергии активации следует, что для стали, прошедшей МТО, и для стали в закаленном состоянии диффузионные процессы контролируются одними и теми же факторами. [25]
 |
Второй момент спектров ЯМР 1SF в CsIrF6 ( 1, RbIrF6 ( 2 и KIrF0 ( 3. [26] |
Подставляя экспериментальные данные по зависимости S2 ( p), находим для CsIrF6 Р 1 2 - 10 - 5 бар-1. На рис. 39 представлена зависимость энергии активации движения в CsIrF6 как функция расстояния катион - комплексный аннон. Здесь же даны рассчитанные значения энергии решетки для CsIrF6, RbIrF6 и KIrF6 как функции междуионного расстояния. Сравнение показывает, что основной вклад в изменение высоты барьеров для движения в CsIrFe действительно вносит сокращение расстояния цезий - гексафторокомплекс и что замена катионов до некоторой степени эквивалентна приложению внешнего гидростатического давления. [27]
Для оценки величин взаимодействий белок - вода менее трудоемким способом были проведены следующие приближенные вычисления. На основании предположения, что молекула белка обладает уникальной фиксированной структурой, определяемой методами рентгеновской кристаллографии, рассчитываются взаимодействия между белком и единственной молекулой воды в отсутствие других молекул растворителя. После этого для данной простой системы можо рассмотреть поочередно все положения и ориентации единственной молекулы воды относительно белка. Рассчитанные значения энергии, представленные в виде трехмерной карты, весьма информативны в отношении описания пространства, занятого в кристалле растворителем. Принималось, что одна треть объема кристалла заполнена растворителем. [28]
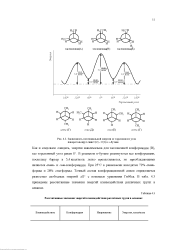 |
Зависимость потенциальной энергии от торсионного угла поворотавокруг сваи С ( 2 - С ( 3 в н-бутане.| Рассчитанные значения энергий взаимодействия различных групп в алканах. [29] |
В реальном н-бутаие реализуются все конформаиии, поскольку барьер в 5 4 ккал / моль легко преодолевается, но преобладающими являются анти - и гоги-конформации. При 25 С в равновесии находятся 72 % антиформы и 28 % гоги-формы. Точный состав конформациониой смеси определяется разностью свободных энергий дО с помощью уравнения Гиббса. В табл. 4.3 приведены рассчитанные значения энергий взаимодействия различных групп в алкаиах. [30]
Страницы: 1 2 3
