Рассчитанное значение - энергия
Cтраница 3
Полингом составлена шкала электроотрицательности элементов на основе термохимических данных. Для гомоатомных молекул Ъ с С а и вклад ионных канонических форм будет очень мал; для гетероатомных молекул вклад ионных форм А В - и А-В ( в зависимости от электроотрицательности элементов) становится значительным. Энергия ионного резонанса ( разность между экспериментальным значением общей энергии связи и рассчитанным значением энергии ковалентной связи) и определяет разность электроотрицательностей элементов. Поскольку экспериментальное значение энергии связи С1 - F равно 248 9 кДж / моль, то энергия ионного резонанса ( вклад формы C1 F -) составит 51 65 кДж / моль. [31]
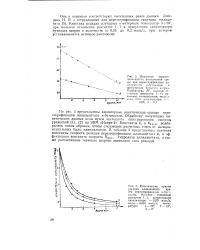
На рис. 3 представлены характерные кинетические кривые переэтерификации аллилацетата н-бутанолом. В таблице 2 представлены значения константы скорости реакции переэтерификации аллилацетата k и эффективная константа скорости / С8Нибл гидролиза аллилацетата, а также рассчитанные значения энергии активации этих реакций. [33]
Найдено, что значение энергии активации, рассчитанное по опытным данным, принимая порядок реакции равным 2 / 3, составляет 46 клал. Значение Е2 оценено в 7 5 ккал ( см. табл. XII. Если принять, что обратная реакция идет без энергии активации, то эта величина может быть принята как минимально возможное значение энергии активации EI. Тогда рассчитанное значение энергии активации цепного разложения будет равно 48 7 ккал - 772 48 ккал при 800 К, что хорошо совпадает с данными опытов. Эмпирические данные Леторта по скорости реакции могут быть представлены в виде уравнения ( XIII. [34]
А - В V2 ( А - A - f - В - В), где А - В, А - - А и В - - В означают энергии связи молекул АВ, АА и ВВ. Например, энергия связи Н2 составляет 4 45 12 - 1 54 и F2 - 2 80 эв на молекулу. Отсюда, согласно сделанному предположению, рассчитывается энергия, которая приходится на гомеополяр-ную долю связи для HI 3 00, для HF 3 63 эв. Экспериментально найденные значения энергии связи составляют 3 07, соответственно 6 39 эв. В случае HI рассчитанное значение только немного отклоняется от экспериментально найденного; в этом случае существует, следовательно, почти чистая гомеополярная связь, о чем свидетельствуют также многие свойства соединения. Напротив, для HF рассчитанное значение энергии связи намного меньше экспериментально найденного. [35]
Например, энергия связи Н2 составляет 4 45 12 - 1 54 и F2 - 2 80 зв на молекулу. Отсюда, согласно сделанному предположению, рассчитывается энергия, которая приходится на гомеополяр-ную долю связи для HI 3 00, для HF 3 63 эв. Экспериментально найденные значения энергии связи составляют 3 07, соответственно 6 39 эв. В случае HI рассчитанное значение только немного отклоняется от экспериментально найденного; в этом случае существует, следовательно, почти чистая гомеополярная связь, о чем свидетельствуют также многие свойства соединения. Напротив, для HF рассчитанное значение энергии связи намного меньше экспериментально найденного. Отсюда Полинг сделал заключение, что в этом случае значительная доля энергии связи ( 2 76 ав, следовательно, около 43 %) приходится на гетерополярную часть связи, что также хорошо согласуется со свойствами этого соединения, которые свидетельствуют о его сильно полярном характере. [36]
Если в принципе в каждой связи существуют квантово-механические силы взаимодействия ( притяжение или отталкивание) и лишь при этом условии на них накладывается притяжение, возникающее между противоположно заряженными ионами, то становится ясным, что это дополнительное действие ионной связи только увеличивает прочность связи, но никогда не может понизить ее. Используя представление о таком наложении, Полинг указал метод, при помощи которого для случаев так называемых смешанных гомео - и гетерополярных соединений, расположенных между экстремальными типами соединений, можно приблизительно рассчитать часть энергии связи, приходящуюся на ионную связь. А - - - В 1 / 2 ( А - - - А В - - - В), где А - - - В, А - - - А и В ч - В означают энергии связи молекул АВ, АА и ВВ. Например, энергия связи Н2 составляет 4 45, 12 - 1 54 и F2 - 2 80 эв на молекулу. Отсюда, согласно сделанному предположению, рассчитывается энергия, которая приходится на гомеополярную долю связи для HI 3 00, для HF 3 63 эв. Экспериментально найденные значения энергии связи составляют 3 07, соответственно 6 39 эв. В случае HI рассчитанное значение только немного отклоняется от экспериментально найденного; в этом случае существует, следовательно, почти чистая гомеополярная связь, о чем свидетельствуют также многие свойства соединения. Напротив, для HF рассчитанное значение энергии связи намного меньше экспериментально найденного. Отсюда Полинг сделал заключение, что в этом случае значительная доля энергии связи ( 2 76 эв, следовательно, около 43 %) приходится на гетерополярную часть связи, что также хорошо согласуется со свойствами этого соединения, которые свидетельствуют о его сильно полярном характере. [37]
Эти условия удовлетворяют требованиям цепной реакции Н2 Вг2, и можно ожидать, что цепные реакции с участием 12 и С12 идут по аналогичному механизму. Величина AtS i 2 примерно одинакова для всех галогенов. Следовательно, можно ожидать, что основные различия реакций и обусловлены различной величиной энергии активации. Энергия активации реакции С1 Н2 НС1 Н равна примерно 6 ккал, так что суммарная цепная реакция будет иметь энергию активации, равную 35 ккал. Это на 5 ккал меньше, чем энергия активации реакции H2 - j - Br2, и при 180 скорости этих реакций отличаются в 260 раз. Энергии активации для фотолиза: 6 ккал для С12, 17 6 ккал для Вг2; рассчитанное значение энергии активации для 12 составляет 35 ккал. В этом случае уже нельзя пренебрегать реакциями обрыва цепи, такими, как H F M и Н Н М, по сравнению с F F - f - М и алгебраические выражения для скорости реакции становятся более сложными. Эта реакция является одной из наиболее экзотермических реакций ( на единицу веса реагирующего вещества) и используется для того, чтобы получить интенсивные пламена. [38]
Эти условия удовлетворяют требования цепной реакции Н2 Вг2, и можно ожидать, что цепные реакции с участием 13 и С12 идут по аналогичному механизму. Величина & Sii2 примерно одинакова для всех галогенов. Следовательно, можно ожидать, что основные различия реакций и обусловлены различной величиной энергии активации. Энергия активации, реакции С1 Н2 - - НС1 - - Ы равна примерно 6 ккал, так что суммарная цепная реакция будет иметь энергию активации, равную 35 ккал. Это на 5 ккал меньше, чем энергия активации реакции Н2 Вг2, и при 180 скорости этих реакций отличаются в 260 раз. Энергии активации для фотолиза: 6 ккал для С12, 17 6 ккал для Вг2; рассчитанное значение энергии активации для 12 составляет 35 ккал. В этом случае разница в энергиях активации более существенна, а. В этом случае уже нельзя пренебрегать реакциями обрыва цепи, такими, как H F - j - M и Н Н М по сравнению с F F M и алгебраические выражения для скорости реакции становятся более сложными. Эта реакция является одной из наиболее экзотермических реакций ( на единицу веса реагирующего вещества) и используется для того, чтобы получить интенсивные пламена. [39]
Страницы: 1 2 3