Свертывание - белок
Cтраница 3
По этой причине исследование механизма укладки цепи дисульфидсодержа-щего белка может иметь ограниченное значение для свертывания белков без таких мостиков. [31]
При воздействии ЛИ в непрерывном режиме преобладают в основном тепловые эффекты, следствием которых являются свертывания белка, а при больших мощностях-испарение биоткани. [32]
 |
Факторы, определяющие биологические изменения ( при лазерном облучении. [33] |
При воздействии непрерывного лазерного излучения преобладает в основном тепловой механизм действия, в результате которого происходит свертывание белка, а при больших мощностях - испарение биоткани. При импульсном режиме ( с длительностью импульсов меньше 10 - 2 с) механизм взаимодействия становится более сплошным и приводит к преобразованию излучения в энергию механических колебаний среды, в частности ударной волны. При мощности излучения свыше 107 Вт и высокой степени фокусировки лазерного луча возможно возникновение ионизирующих излучений. [34]
Большинство методов определения белка в моче, как качественных, так и количественных, основано на возможности свертывания белков с превращением их в нерастворимую в воде форму. Техника выполнения проб на белок ( проба Геллера, проба кипячением с уксусной кислотой, реакция с сульфосалициловой кислотой и др.) подробно описывается в практических руководствах по биологической химии. [35]
Большинство методов определения белка в моче, как качественных, так и количественных, основано на возможности свертывания белков с превращением их в нерастворимую в воде форму. Техника выполнения пробна белок ( проба Геллера, проба кипячением с уксусной кислотой, реакция с сульфосалициловой кислотой и др.) подробно описывается в практических руководствах по биологической химии. [36]
Однако процесс свертывания апомиоглобина происходит намного быстрее, и поэтому можно предположить его большую направленность по сравнению со свертыванием дисульфидсодержащих белков ( разд. [37]
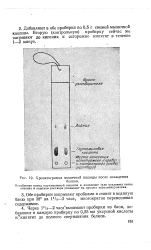 |
Хроматограмма мышечной кашицы после осаждения. [38] |
Через Wa-2 часа вынимают пробирки из бани, добавляют в каждую пробирку по 0 25 мл уксусной кислоты накипятят до полного свертывания белков. [39]
Вызвать осаждение белков из растворов можно различными способами, например прибавлением солей ( сернокислого аммония и др.), кислот, спирта, а также нагреванием, при котором происходит свертывание белка. В зависимости от того, чем вызвано осаждение, а также от характера самого белка, осадок белка может оказаться мало или, наоборот, - сильно измененным. Осаждение солями в большинстве случаев приводит к наименьшим изменениям: осадок, полученный при прибавлении солей, обычно можно опять растворить и раствор в большинстве случаев будет обладать прежними свойствами. Другие способы осаждения, например нагревание ( кипячение), приводят к более глубоким изменениям: свернувшийся при кипячении белок при обычных условиях уже более не растворяется. [40]
Вызвать осаждение белков из растворов можно различными путями, например прибавлением солей ( сернокислого аммония и др.), кислот, пирта, а также нагреванием, при котором происходит свертывание белка. [41]
Вызвать осаждение белков из растворов можно различными путями, например прибавлением солей ( сульфата аммония и др.), кислот, спирта, а также нагреванием, при котором происходит свертывание белка. В зависимости от того, чем вызвано осаждение, а также в зависимости от характера самого белка, осадок белка может оказаться мало измененным или же сильно измененным. Осаждение солями в большинстве случаев приводит к наименьшим изменениям: осадок, полученный при прибавлении солей, обычно можно опять растворить, и раствор в большинстве случаев будет обладать прежними свойствами. Другие способы осаждения, как, например, нагревание ( кипячение), приводят к более глубоким изменениям: свернувшийся при кипячении белок уже при обычных условиях более не растворяется. [42]
Вызвать осаждение белков из растворов можно различными путями, например прибавлением солей ( сульфата аммония и др.), кислот, спирта, а также нагреванием, при котором происходит свертывание белка, В зависимости от того, чем вызвано осаждение, а также в зависимости от характера самого белка, осадок белка может оказаться мало измененным или же сильно измененным. Осаждение солями в большинстве случаев приводит к наименьшим изменениям: осадок, полученный при прибавлении солей, обычно можно опять растворить, и раствор в большинстве случаев будет обладать прежними свойствами. Другие способы осаждения, как, например, нагревание ( кипячение), приводят к более глубоким изменениям: свернувшийся при кипячении белок уже при обычных условиях более не растворяется. [43]
Лучше объясняет механизм отравления живых организмов другая теория, по которой отравление происходит в результате попадания ионов ртути и меди в органы дыхания или пищеварения, в результате чего происходит свертывание белка этих органов и организм погибает. По данным этой теории защитное действие окиси ртути и закиси меди объясняется следующим образом. Вследствие диффузии морской воды в красочную пленку окись ртути и закись меди подвергаются воздействию NaCl, содержащегося в морской воде. Раствор этой соли, содержащий ионы ртути и меди, медленно диффундируя в направлении обратном диффузии воды, создает в непосредственной близости к судну зону, ядовитую для представителей морской фауны, Эта зона становится ядовитой, как было указано выше, уже при незначительном содержании в воде ионов ртути и меди. При таком механизме действия окиси ртути и закиси меди все простейшие животные организмы, попавшие в зону, отравленную ионами ртути и меди, гибнут и к судну могут случайно подойти только отдельные их экземпляры. Сплошное же обрастание может начаться только после значительного обеднения наружного слоя краски ртутью и медью. На практике такое течение процесса обрастания судна и наблюдается - обрастание начинается с поселения отдельных экземпляров молюсков, а сплошное обрастание, значительно менее интенсивное, чем при применении обычной краски, начинается значительно позже, чем в случае окраски судна обычной масляной краской. [44]
Страницы: 1 2 3