Свойство - заместитель
Cтраница 1
Свойство заместителя оттягивать электронную плотность предполагается неизменным, а влияние этого явления на скорость реакции зависит от ее типа и условий. Если для кислотной диссоциации и еще для некоторых реакций оттягивание электронной плотности от реакционного центра приводит к облегчению процесса, то в других случаях, наоборот, это тормозит реакцию. [1]
Кронных свойств заместителей, надо полагать, что реакция идет по радикальному механизму. [2]
Свойством заместителей I рода является способность подавать электроны, поэтому их называют электронодонорными заместителями. Заместители II рода, наоборот, склонны оттягивать на себя ( принимать) электроны и называются поэтому электроноакцепторными заместителями. [3]
Эти свойства заместителей находятся в соответствии с известным упрощенным правилом: если имеющийся в ядре заместитель не содержит кратных связей ( заместители первого рода), то вступающий заместитель направляется в орто - и пара-положения; ненасыщенные группы ( заместители второго рода) приводят к преимущественному образованию лшпа-производных. Ориентация вступающего заместителя обычно определяется кинетикой реакции: это значит, что существуют три конкурирующих процесса ( орто -, мета и пара-замещение), протекающих с различной скоростью. В согласии с этим процессы электрофильного замещения в аренах прекрасно коррелируются с помощью уравнения Гаммета. Поскольку реакционный центр электронно не изолирован от первого заместителя, нужно использовать величины а ( см. гл. [4]
Усиление электроиодонорных свойств заместителя R в пиридиновом ядре и перемещение его из J3 - в Y-положение уменьшает электрофильные свойства а-углеродов и, значит, усиливает противодействие нуклео-фильной атаке размыкающего амина. Рамзай ( 1877 г.) получил пиридин измененным синтезом Бертло ( стр. [5]
Строение и свойства заместителя, вытесняемого при нуклеофильной атаке, могут оказывать существенное влияние на суммарную скорость реакции. [6]
Естественно, что донорноакцепторные свойства заместителей, в свою очередь, оказывают значительное влияние на химическое поведение и самой системы полисопряжения. [7]
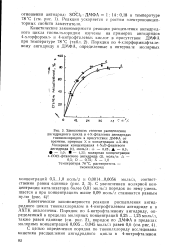 |
Зависимость степени расщепления. ангидридного цикла в 4 - Х - фталевых ангидридах. [8] |
Реакция ускоряется с торных свойств заместителя. [9]
Как видно, строение и свойства вытесняемого заместителя очень сильно влияют на скорость нуклеофильного замещения, изменяя ее на 5 - 6 порядков. Этот эффект является суммарным. Он складывается из влияния заместителя на скорость образования а-комп-лекса и на скорость его разрушения с образованием конечного продукта. Как уже сообщалось, скорость образования сг-комплекса зависит от электрофильности реакционного центра субстрата, на которую влияет индуктивный эффект заместителя. Скорость отрыва вытесняемого заместителя зависит прежде всего от его нуклеофиль-ности, но также и от условий в которых проводится реакция, которые могут содействовать или препятствовать стабилизации образующегося аниона. [10]
Как видно, строение и свойства вытесняемого заместителя очень сильно влияют на скорость нуклеофильного замещения, изменяя ее на 5 - 6 порядков. Этот эффект является суммарным. Он складывается из влияния заместителя на скорость образования а-комп-лекса и на скорость его разрушения с образованием конечного продукта. Как уже сообщалось, скорость образования а-комплекса зависит от электрофильности реакционного центра субстрата, на которую влияет индуктивный эффект заместителя. Скорость отрыва вытесняемого заместителя зависит прежде всего от его нуклеофиль-ности, но также и от условий в которых проводится реакция, которые могут содействовать или препятствовать стабилизации образующегося аниона. [11]
Слабая зависимость скорости обмена от свойств заместителя, проявляющаяся в небольшой величине наклона прямой Бренстедовского графика, показывает, что процесс обмена близок к синхронному. [12]
Для количественной оценки электроноактнвных н стерео-химических свойств заместителей предложено большое число различных шкал. [13]
Различие же в размерах и свойствах внешне-сферных заместителей - щелочных металлов - позволяет объяснить увеличение устойчивости комплексных соединений в ряду К-Rb - Cs. Таким образом, рассматривая выделенные нами соединения как комплексные, можно объяснить изменение устойчивости этих соединений. Следовательно, полученные нами результаты по изучению систем типа МеНа. [14]
Страницы: 1 2 3 4
