Свойство - раствор - электролит
Cтраница 3
В ряде работ [51-59] изучались свойства растворов электролитов типа МХ2 - MX - Н2О, где X - ион галогена или перхлорат-ион, М2 - ион элемента второй группы и М - ион водорода или щелочного металла. [31]
Изменение потенциала гр определяет зависимость свойств растворов электролитов ( коэффициентов активности, осмотических коэффициентов, коэффициентов электропроводности и др.) от концентрации. [32]
Изменение потенциала ф определяет зависимость свойств растворов электролитов от концентрации: коэффициентов активности, осмотических коэффициентов, коэффициентов электропроводности и других свойств растворов электролитов. [33]
Изменение потенциала ф определяет зависимость свойств растворов электролитов ( коэффициентов активности, осмотических коэффициентов, коэффициентов электропроводности и др.) от концентрации. [34]
Электрохимия изучает некоторые особенности в свойствах растворов электролитов, электропроводность растворов, процессы электролиза, работу гальванических элементов и электрохимическую коррозию металлов. [35]
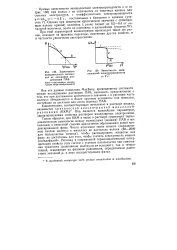 |
Зависимость поверхностного натяжения от логарифма концентрации ПАВ. ККМ - критическая концентрация мицеллообразования.| Зависимость эквивалентной электропроводности. [36] |
Она является важнейшим параметром, характеризующим свойства растворов мицеллярных электролитов. [37]
Наряду с удельной электропроводностью при изучении свойств растворов электролитов широко используют эквивалентную электропроводность, пред ставляющую собой проводимость плоского слоя раствора электролита толщиной в 1 см, содержащего грамм-эквивалент растворенного вещества. [38]
Экспериментально а определяют, наблюдая отклонения свойств растворов электролитов от теоретических зависимостей, установленных для идеальных растворов. [39]
Электролитическая диссоциация проявляется в сильном отклонении свойств растворов электролитов от идеальности. [40]
Экспериментально а определяют, наблюдая отклонении свойств растворов электролитов от теоретических зависимостей, установленных для идеальных растворов. [41]
Экспериментально а определяют, наблюдая отклонения свойств растворов электролитов от теоретических зависимостей, установленных для идеальных растворов. [42]
Термодинамические функции, используемые при анализе свойств растворов электролитов, обычно в той или иной форме учитывают происходящие в этих растворах химические процессы. При термодинамической же обработке данных, характеризующих свойства растворов неэлектролитов, эти химические факторы обычно непосредственно не учитываются. [43]
Электролитическая диссоциация проявляется в сильном отклонении свойств растворов электролитов от идеальности. [44]
При этом был использован принцип аддитивности свойств растворов электролитов, несколько отличающийся от принципов равной ионной силы или равной активности воды, лежащих в основе методов Юнга и Здановского. Мы исходили из предположения, что объем смешанного раствора будет равен сумме объемов бинарных растворов в том случае, если вода имеет во всех исходных растворах одинаковый парциальный молярный объем. При этом химическое взаимодействие ( нейтрализация, выпадение осадка, комплексообразование) между смешиваемыми исходными растворами должно отсутствовать. [45]
Страницы: 1 2 3