Свойство - разбавленный раствор
Cтраница 1
Свойства разбавленных растворов, зависящие только от концентрации растворенного вещества. [1]
Свойства разбавленных растворов, зависящие только от количества нелетучего растворенного вещества, называются коллигативными свойствами. К ним относятся: понижение давление пара растворителя над раствором, повышение температуры кипения и понижение температуры замерзания раствора, а также осмотическое давление. [2]
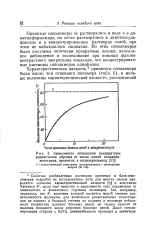 |
Зависимость понижения температуры. [3] |
Свойства разбавленных растворов привитых и блок-сополимеров подробно не исследовались) хотя для многих систем приводятся значения характеристической вязкости [ TJ ] и константы Хаггинса k, мало еще известно о зависимости этих параметров от химического и физического строения полимеров. Так, например, оказалось, что k, величина которой является мерой степени разветвленное молекулы, для нескольких разветвленных полистиро-лов не зависит в большой степени от наличия в полимере небольшого количества длинных боковых цепей, но сильно зависит от наличия большого числа коротких боковых цепей. [4]
На свойства разбавленных растворов влияют в основном два фактора: природа растворителя и растворенного вещества и концентрация. Исходя из этого, растворы обладают следующими характерными свойствами: 1) давление пара раствора ниже давления пара растворителя; 2) растворы замерзают при более низкой температуре, чем их растворители; 3) растворы кипят при более высокой температуре, чем их растворители. [5]
 |
Связь между понижением давления пара и понижением температуры замерзания. [6] |
На свойства разбавленных растворов влияют в основном два фактора: природа растворителя и растворенного вещества и концентрация. [7]
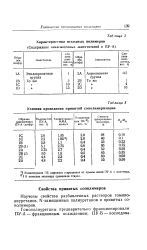 |
Характеристика исходных полимеров.| Условия проведения привитой сополимеризации. [8] |
Изучены свойства разбавленных растворов гомопо-лиуретанов, N-замещенных полиуретанов и привитых сополимеров. [9]
Обычно свойства разбавленных растворов электролитов делят на две группы. К первой группе относят свойства, не зависящие для данного растворителя от природы растворенного вещества. Это давление насыщенного пара растворителя над раствором, повышение температуры кипения и понижение температуры затвердевания по сравнению с растворителем, осмотическое давление и др. Проявление растворами таких свойств послужило основой для создания физической теории растворов. [10]
Изучение свойств разбавленных растворов представляет не только теоретический, но и практический интерес. Достаточно напомнить о возможности определения молекулярной массы и о-том, что нередко приходится иметь дело с растворами плохо растворимых веществ, которые сама природа сделала очень разбавленными. Кроме того, хотя уравнения (IV.4), (IV.6), (IV.7) и (IV.9), отражающие предельные законы, как и закон Генри, относятся к разведенным ( строго говоря, к бесконечно разведенным) растворгм, однако с некоторой погрешностью ими можно пользоваться и п эи умеренном разбавлении. Для концентрированных же растворов, где они совершенно неприменимы, ими можно воспользоваться для грубой ориентировки, что тоже небесполезно. [11]
Изучение свойств разбавленных растворов представляет не только теоретический, но и практический интерес. Достаточно напомнить о возможности определения молекулярного веса и о том, что нередко приходится иметь дело с растворами плохо растворимых веществ, которые сама природа сделала очень разбавленными. Кроме того, хотя уравнения (IV.4), (IV.6), (IV.7) и (IV.9), отражающие предельные законы, как и закон Генри, относятся к разведенным ( строго говоря, к бесконечно разведенным) растворам, однако с некоторой погрешностью ими можно пользоваться и при умеренном разбавлении. Для концентрированных же растворов, где они совершенно неприменимы, ими можно воспользоваться для грубой ориентировки, что тоже небесполезно. [12]
Ниже рассмотрены четыре свойства разбавленных растворов. [13]
 |
Равновесие жидкость - пар ( схема. [14] |
Ниже рассмотрены четыре свойства разбавленных растворов. [15]
Страницы: 1 2 3 4