Свойство - разбавленный раствор
Cтраница 3
В уравнениях (IV.3), (IV.6), (IV.9) для свойств разбавленных растворов предполагается, что вторая фаза ( пар или кристаллы) образуется только за счет молекул растворителя. Поэтому эбулио-метрическим методом можно пользоваться только для растворов практически нелетучих веществ, а криометрическим методом - - только для растворов веществ, которые не образуют с растворителем смешанных кристаллов. [31]
Тот же коэффициент i входит в другие уравнения для свойств разбавленных растворов. [32]
 |
Химический потенциал. [33] |
Таким образом, уравнением (5.12) можно пользоваться для описания свойств идеальных разбавленных растворов только в тех интервалах концентраций, в которых оно сохраняет свою силу. При более высоких концентрациях следует учитывать отклонения от идеальности, но этот вопрос в данной главе рассматриваться не будет. [34]
Следует, однако, заметить, что аналогия в свойствах разбавленных растворов и идеальных газов является далеко не полной, так как характер движения молекул растворенного вещества в жидкости значительно отличается от движения молекул газа. [35]
Газовая теория растворов дает ряд простых количественных зависимостей, удовлетворительно описывающих свойства разбавленных растворов. [36]
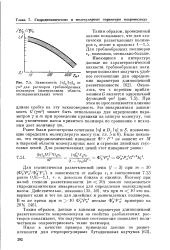 |
Зависимость [ т ] ] р / [ т ] ] л от уто2 для растворов гребнеобразных полимеров ( заштрихована область экспериментальных точек. [37] |
Таким образом, данные о влиянии параметров длинноцепной разветвленности макромолекулы на свойства разбавленных растворов показывают, что полученные соотношения позволяют количественно охарактеризовать такие полимеры. [38]
Экспериментальные данные показывали, что в большинстве случаев положение об аддитивности свойств разбавленных растворов распространяется на электропроводность, температуру замерзания, теплоту нейтрализации, рефракцию и другие свойства электролита. [39]
Это обстоятельство может объяснить ряд неожиданных успехов модели Рауза в интерпретации некоторых свойств разбавленных растворов. [40]
Физическая точка зрения на растворы основывалась на том, что целый ряд свойств разбавленных растворов: осмотическое давление, упругость паров и др., зависит от соотношения количества молекул составных частей и мало зависит от их природы. [41]
Аррениус обратил большое внимание на доказательство того положения, что большая часть свойств разбавленных растворов электролитов относится к аддитивным свойствам. [42]
В основе наиболее широко распространенных физических методов определения молекулярных весов полимеров лежит изучение свойств разбавленных растворов. Методы, подробно рассмотренные в предыдущих главах - - вискозиметрический, осмометрический, криоскопический, эбулиоскопический, седиментационный, оптический ( по светорассеянию в растворах) - являются типичными примерами. [43]
Теория сильных электролитов, учитывающая электростатическое взаимодействие между ионами в растворе, количественно описывает свойства разбавленных растворов. [44]
Для большинства полимеров достаточно точное измерение их средних ММ и ММР основано на исследовании свойств разбавленных растворов. Однако многие полимеры невозможно анализировать ни одним из этих методов вследствие их нерастворимости. Ряд методов оценки средних молекулярных масс и вида ММР плавких линейных полимеров может быть предложен на основе исследования взаимосвязи молекулярно-мас-совых и реологических характеристик расплавов полимеров. Основными факторами, определяющими вязкостные и вязко-упругие свойства расплавов полимеров, являются ММ и ММР. [45]
Страницы: 1 2 3 4