Свойство - смешанный раствор
Cтраница 1
Свойства смешанных растворов моноам-монийфосфат - фторид аммония - вода и диаммонийфосфат - фторид аммония - вода представляют интерес в связи с возможностью получения фосфатов аммония путем взаимодействия фторапатита кальция с водными растворами фторида аммония. [1]
Свойства смешанных растворов систем моноаммонийфос-фат - фторид аммония - вода и диаммонийфосфат - фторид аммония - вода представляют практический интерес в связи с возможностью получения фосфатов аммония, используя водные растворы фторида аммония. [2]
Некоторые свойства смешанных растворов, подчиняющихся правилу Здановского ( удельный объем, теплоемкость, растворимость и др.), складываются аддитивно из свойств бинарных растворов с тем же давлением паров воды. [3]
Расчетное определение свойств смешанных растворов возможно, например, на основе принципа аддитивности. В простейшем случае принцип аддитивности заключается в том, что численное значение некоторой функции одного или нескольких свойств смешанного раствора равно сумме произведений численных значений функций этих свойств для бинарных растворов, из которых можно образовать смешанный раствор, на их относительную долю в смеси. [4]
 |
Схема расположения изоактиват воды на диаграммах растворимости систем X - Z - Н20 и Y - Z - Н20. [5] |
Принципу обобщенной аддитивности удовлетворяют свойства разбавленных смешанных растворов, являющиеся функцией от ионной силы раствора. Вопрос о том, обладают ли свойства концентрированных растворов обобщенной аддитивностью, может быть решен лишь опытным путем. [6]
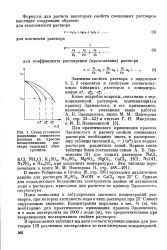 |
Схема условного разделения смешанного раствора на простые изопиестические растворы отдельных электролитов. [7] |
Для практического применения правила Здановского к расчету свойств смешанных растворов необходимо иметь в распоряжении таблицы значений аю f ( а) для водных растворов различных солей. [8]
После этих определений вычисляют по соответствующим аддитивным формулам значение свойств смешанного раствора. [9]
Для растворов, удовлетворяющих принципу аддитивности, имеется возможность вычислить свойства смешанных растворов электролитов по численным данным о свойствах бинарных растворов каждого из этих электролитов в отдельности при тех же температуре и давлении. При отсутствии обобщенной аддитивности количественное определение свойств смешанных растворов возможно только опытным путем. [10]
Развита термодинамическая теория четырехкомпонентных растворов электролитов, подчиняющихся правилу Здановского об аддитивности свойств смешанных растворов. Выведены формулы для расчета коэффициентов активности в растворах трех солей с общим ионом, в том числе с учетом неодинакового влияния солей на свойства других солей, присутствующих в растворе. [11]
 |
Диаграмма изменения коэффициента активности КС1 в смешанном водном растворе КС1 и NaCl при 25 С. [12] |
В нашей работе [8] мы определили понятие обобщенной аддитивности значительно шире, как принципиальную возможность вычисления свойств смешанного раствора по численным данным о свойствах бинарных растворов каждого из этих электролитов в отдельности при тех же температурах и давлении. При отсутствии аддитивности в этом смысле количественное определение свойств смешанных растворов возможно только опытным путем. [13]
А находят по справочным таблицам значения свойств бинарных растворов, и по соответствующим аддитивным формулам [18] вычисляются значения свойств смешанного раствора. [14]
Однако, как показал Микулин [33], правило Харнеда имеет ограниченный характер и его можно считать пригодным для описания свойств смешанных растворов электролитов лишь в отдельных частных случаях. Как правило, уравнение Харнеда можно применять лишь для малых концентраций, а попытки использования его для анализа свойств концентрированных растворов не могут дать положительных результатов. [15]
Страницы: 1 2 3