Свойство - смешанный раствор
Cтраница 2
Развита термодинамическая теория четверных водных взаимных систем, состоящих из солей, тройные растворы которых подчиняются правилу Здановского об аддитивности свойств смешанных растворов. Показано, что для таких систем изоактиваты воды в общем случае не прямолинейны и являются отрезками гипербол. [16]
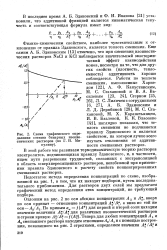 |
Схема графического определения состава бинарных изопие-стических растворов ( по Г. И. Ми-кулину. [17] |
В этой работе мы развиваем термодинамическую теорию растворов электролитов, подчиняющихся правилу Здановского, и, в частности, ищем пути разрешения трудностей, связанных с экстраполяцией в область сверхпересыщенных растворов, неизбежной при применении правила Здановского к расчету свойств концентрированных смешанных растворов. [18]
Оказывается, если смешивать растворы с одинаковой упругостью паров ( или, что то же самое, с одинаковыми активностями воды в растворе), когда растворенные соли химически не взаимодействуют ( например КС1 и NaCl, NaCl и MgCI2), упругость паров смешанного раствора, в пределах точности эксперимента, будет равна упругости паров смешиваемых растворов. Некоторые свойства смешанного раствора ( объем, удельный вес, теплоемкость и др.) складываются аддитивно из свойств исходных растворов отдельно взятых солей. [19]
Если численные постоянные, входящие в теоретические формулы для смешанных растворов и вычисленные по опытным данным, складываются по принципу обобщенной аддитивности из соответствующих постоянных для бинарных растворов отдельных электролитов, входящих в состав смеси, то зто говорит в пользу справедливости этих формул. Правильное предвычисление свойств смешанных растворов должно явиться вторым важнейшим доказательством справедливости той или иной теории растворов. [20]
Для растворов, удовлетворяющих принципу аддитивности, имеется возможность вычислить свойства смешанных растворов электролитов по численным данным о свойствах бинарных растворов каждого из этих электролитов в отдельности при тех же температуре и давлении. При отсутствии обобщенной аддитивности количественное определение свойств смешанных растворов возможно только опытным путем. [21]
Коэффициенты этого разложения не зависят от ионной силы, и их следует рассматривать как величины, специфические для данной пары электролитов, образующих смешанный раствор. Они определяются по экспериментальным данным о свойствах смешанных растворов. [22]
В нашей работе [8] мы определили понятие обобщенной аддитивности значительно шире, как принципиальную возможность вычисления свойств смешанного раствора по численным данным о свойствах бинарных растворов каждого из этих электролитов в отдельности при тех же температурах и давлении. При отсутствии аддитивности в этом смысле количественное определение свойств смешанных растворов возможно только опытным путем. [23]
Основной проблемой количественной теории смешанных растворов электролитов является вопрос об аддитивности их свойств. Как известно, свойства называются аддитивными, если числовое значение свойства смешанного раствора равно сумме произведений числовых значений того же свойства бинарных растворов на их относительную долю в смеси. Кожуховскому [49], принцип аддитивности свойств раствора выражается в том, что числовое значение некоторой функции одного или нескольких свойств раствора равно сумме произведений числовых значений таких же функций от тех же свойств составляющих веществ на их концентрации в молярных, весовых или объемных долях. [24]
Одной из важнейших задач теории растворов электролитов является установление количественных закономерностей между значениями величин термодинамических свойств ( коэффициенты активности и осмотический, энтальпия и энтропия, удельный объем и теплоемкость, сжимаемость и тепловое расширение) концентрированных водных растворов и концентрацией электролита. Решение этой задачи значительно бы продвинуло вперед представления о природе растворов и позволило предвычислять свойства смешанных растворов и кривые растворимости, что имеет важное практическое значение для технологии переработки водных и неводных растворов минеральных веществ. [25]
Расчетное определение свойств смешанных растворов возможно, например, на основе принципа аддитивности. В простейшем случае принцип аддитивности заключается в том, что численное значение некоторой функции одного или нескольких свойств смешанного раствора равно сумме произведений численных значений функций этих свойств для бинарных растворов, из которых можно образовать смешанный раствор, на их относительную долю в смеси. [26]
Расчетное определение смешанных растворов возможно, например, на основе принципа аддитивности. В простейшем случае принцип аддитивности заключается в том, что численное значение некоторой функции одного или нескольких свойств смешанного раствора равно сумме произведений численных значений функций этих свойств для бинарных растворов ( из которых можно образовать смешанный раствор) на их относительную долю в смеси. [27]
В работе [1], посвященной термодинамике гидратной теории бинарных растворов сильных электролитов, дан обзор развития количественных зависимостей, связанных с гидратной теорией. Распространение этих зависимостей на смешанные растворы началось с 1954 г., когда Г. И. Никулин в работе об аддитивности свойств смешанных растворов солей [2] вывел формулу для свободной энтальпии смешанных растворов и применил ее для предвычисления их свойств по численным данным о свойствах бинарных водных растворов каждого из электролитов в отдельности. Им были построены расчетным путем несколько кривых совместной растворимости в воде двух солей с общим ионом, хорошо совпавших с экспериментальными данными. [28]
В общем случае [ см. уравнение (1.3) ] экстракцию проводят из многокомпонентных растворов. Активность компонентов экспериментально определена лишь для ограниченного круга систем, поэтому значительный практический интерес представляют методы количественного описания свойств смешанных растворов по данным, полученным для бинарных систем. [29]
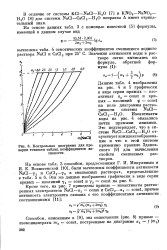 |
Контрольная диаграмма для проверки точности таблиц коэффициентов активности. [30] |
Страницы: 1 2 3