Свойство - фермент
Cтраница 1
Свойства ферментов изучаются in vitro. Многие ферменты получены в кристаллической форме. [1]
Свойство ферментов разрушаться при кипячении является характерной особенностью, отличающей ферменты от других катализаторов, и называется термолабильноетью ферментов. После непродолжительного кипячения ферменты теряют способность проявлять каталитическое действие. Потеря каталитической активности при кипячении обусловлена денатурацией фермента. Сухие препараты ферментов выдерживают нагревание до 100 без заметной потери активности. При низких температурах ферменты хорошо сохраняются. Повышение и понижение температуры сильно изменяют скорость ферментативной реакции. [2]
Свойства ферментов изучены пока недостаточно полно, тем не менее уже сейчас можно отметить некоторые особенности, отличающие эластазы актиномицетов от свиной панкреатической эластазы. [3]
 |
Образование трипсина из трипсиногеиа. [4] |
Свойства ферментов обусловливают эффективность и рентабельность ферментативных препаратов. [5]
Свойства ферментов определяются их белковой природой и биологической ролью. [6]
Эти свойства ферментов обусловлен весьма сложным механизмом их действия, многие стороны которого еще до конца не раскрыты. Представления о механизмах ферментативного катализа получили наиболее существенное развитие лишь в последние 10 - 20 лет. [7]
Такие свойства фермента, как специфичность, величина константы Миха: лнса и оптимальное значение рН при переводе фермента в нерастворимое COCTOJ ние могут несколько измениться. Активность фермента, закрепленного на целль лозной матрице, несколько ниже активности свободного фермента в раствор обычно она составляет 10 - 90 % от исходной активности. При работе возможн также проявление молекулярно-ситового действия целлюлозной основы. [8]
Эти свойства ферментов обусловлены сложной структурой макромолекул белка и сложным механизмом их действия. Механизм этот заключается, в частности, в сорбции субстрата на ферменте и образовании ими активного комплекса в результате гидрофобных, полярных и ионных взаимодействий; в этом комплексе происходит сближение и ориентация реагирующих групп фермента и субстрата. Взаимодействие между ферментом и сорбированным субстратом имеет полифункциональный характер, при котором молекула субстрата подвергается атаке сразу нескольких каталитических групп активного центра фермента, что и обусловливает, в частности, его высокую каталитическую активность. [9]
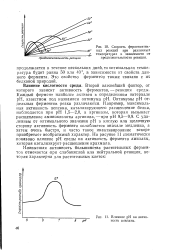 |
Скорость ферментативных реакций при различных температурах в зависимости от продолжительности реакции.| Влияние рН на активность амилазы. [10] |
Это свойство ферментов также связано с их белковой природой. [11]
Они приобретают свойства ферментов после соединения. [12]
Подробное изложение свойств ферментов и катализируемых ими процессов является одной из главных задач курса биологической химии, а потому здесь не приводится. [13]
Изучение некоторых свойств фермента липазы из семян чернушки дамасской / / Химия природ, соедин. [14]
То, что регуляторные свойства ферментов действительно препятствуют накоплению больших количеств субстратов ( и позволяют избежать трудностей, связанных с пределом растворимости и неконтролируемыми реакциями), было ясно продемонстрировано при изучении кратковременных изменений в концентрациях субстратов во время перехода от сравнительно низкой к чрезвычайно высокой интенсивности обмена. [15]
Страницы: 1 2 3 4