Хромофорное свойство
Cтраница 2
Галлий, как элемент, не обладающий хромофорными свойствами, дает цветные реакции только с окрашенными реагентам: и или поглощающими в близкой ультрафиолетовой области спектра. [16]
Фотометрические методы определения содержания алюминия, не обладающего хромофорными свойствами, осуществляют с применением рассмотренных в разделах Алюминий, Титриметрические методы комплексономет-рических индикаторов. [17]
Несмотря на то, что цирконий не обладает хромофорными свойствами, в настоящее время предложены десятки красителей в качестве реагентов, пригодных для его фотометрического определения. Удельный вес фотометрических методов в последние годы начинает резко увеличиваться. Такая тенденция вполне закономерна, если учесть, что фотометрические методы, не уступая по точности весовым и объемным, вместо с тем оказываются более быстрыми. [18]
Комплексен III образует с катионами металлов, обладающими хромофорными свойствами ( например, Fe, Сг, Си, Со, Ш), окрашенные комплексы, что и позволяет применять комплексов III для фотометрического определения этих металлов. [19]
Медь относится к числу тех металлов, которые обладают хромофорными свойствами, поэтому среди многочисленных фотометрических методов определения меди имеются как методы, основанные на использовании окрашенных реагентов с хромофорными группами, так и методы, в которых применяют бесцветные реагенты. Большинство методов обладает высокой селективностью. Это подробно описанные ниже дитизоновый, дитиокарбаматный, купроиновый и купризоновый методы или метод с применением бмс - ( цикло-гексанон) оксалилдигидразона; наибольшей чувствительностью обладает дитпзоновый метод. При помощи купризона определяют медь в водной фазе, остальные перечисленные методы относятся к экстракционно-фотометрическим. [20]
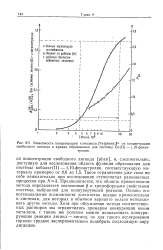 |
Зависимость концентрации комплекса [ Fe ( phen Зр от концентрации свободного лиганда и кривая образования для системы Со ( П - 1 10-фенан. [21] |
Предполагается, что область применимости метода определяется значениями р и хромофорными свойствами системы, выбранной для конкурирующей реакции. Однако его потенциальные возможности достаточно велики применительно к системам, для которых в обычном варианте нельзя использовать другие методы. Хотя при обсуждении метода соответственных растворов мы ограничились примером конкуренции ионов металлов, с таким же успехом можно использовать конкурирующие реакции лиганд - лиганд, но для такого исследования гораздо труднее экспериментально подобрать подходящую пару лигандов. [22]
Диантипирилметан образует окрашенные комплексы аминного типа с некоторыми металлами ( имеющими хромофорные свойства) также в водном растворе. Однако поглощение этих комплексов обычно сдвинуто в сторону ультрафиолета, что менее удобно для фотометрии. Значительная прочность связи Me - Diant приводит к тому, что диантипирилметан нередко замещает ( частично или полностью) атомы кислорода в гидооксо-комплексах или способствует их замещению роданид-ионами. При этом образуются комплексы негидролизованных форм высоковалентных металлов, что значительно увеличивает их хромофопный эффект. Обращает также внимание влияние лигандов, содержащих спиртовые или фенольные группы. Здесь, вероятно, проявляется связь Меп - О, в результате чего такие комплексы окрашены слабее, чем, например, аналогичные им роданиды. [23]
Азогруппа ( - NN - ) содержится в азосоединениях, обладает хромофорными свойствами. [24]
Если сравнить производные мочевины и тиомочевины, то у последнего соединения обнаруживаются более сильные хромофорные свойства. По аналогии с карбонильной группой, для соединений с тионной группировкой ( например, в алифатических тиокетонах) можно предсказать две полосы поглощения, которые должны появиться при значительно больших длинах волн. Интенсивные полосы, вероятно, должны лежать в области 230 - 260 ммк, а более слабые - при 300 - 330 ммк. [25]
Оно кроме того выяснило, при каких условиях этиленная группировка С С приобретает хромофорные свойства. [26]
Окрашенные комплексы диалкил - и диарилдитиофосфаты образуют только с ионами металлов, обладающими хромофорными свойствами. [27]
Тем не менее в общем вопрос о влиянии строения валентных ор-биталей атома металла на хромофорные свойства лиганда значительно сложнее. [28]
Общие представления органической химии о свойствах цепи сопряжения часто позволяют качественно, но надежно оценивать хромофорные свойства реактивов. Ниже рассмотрены три наиболее типичных случая взаимодействия ионов металлов с окрашенными реактивами. [29]
В реальных даже очень чистых полимерах содержатся дефекты структуры и аномалии молекулярного строения, которые обладают хромофорными свойствами. Наличие та ких дефектных хромофоров приводит к тому, что многие технические полимерные материалы поглощают излучение с Яф ЗОО нм. Поэтому они оказываются в сфере фотохимического воздействия солнечной радиации, достигшей поверхности Земли. [30]
Страницы: 1 2 3 4