Металлическое свойство - элемент
Cтраница 1
Металлические свойства элементов третьей группы объясняются легко. [1]
Металлические свойства элементов возрастают справа налево по периодам и сверху вниз по группам. [2]
Металлические свойства элемента нельзя сводить только к его электроположительности и к способности образовать основания; эти свойства являются важнейшими, но не исчерпывают всех металлических свойств. Строго говоря, металличность не является свойством отдельных атомов: она проявляется там, где имеется взаимодействие между атомами. Одним из лучших подтверждений этого является тот факт, что щелочные металлы, ртуть и др. в парообразном состоянии не обладают характерными свойствами металлов. Далее, известно, что не только металлы могут обладать металлическими свойствами. Например, получено вещество состава C3H8Hg2, являющееся хорошим проводником электричества и в прессованном виде отличающееся металлическим блеском ( цвета меди): Наконец, известен ряд соединений металлов с неметаллическими элементами, причем эти соединения также обладают некоторыми свойствами металлов. [3]
Металлические свойства элементов усиливаются от алюминия к таллию. [4]
Металлические свойства элемента, как было сказано ( § 23), зависят от легкости отдачи этим элементом своих валентных элек-тронов. В ряду элементов: N, P, As, Sb, Bi, от первого к последнему все более увеличивается легкость отдачи каждым последующим элементом своих валентных электронов и в таком же порядке ослабляются металлоидные и возрастают металлические свойства этих элементов. Более легкая отдача валентных электронов у последних членов указанного ряда элементов вызвана следующим. У атомов азота и фосфора их валентные электроны находятся ближе к ядру, чем у атомов следующих элементов. Наиболее далеко отстоят от ядра валентные электроны у висмута. Чем дальше отстоят от ядра валентные электроны, тем меньше проявляется сила притяжения между ними и ядром, тем легче отрываются эти электроны от атома и тем больше проявляются металлические свойства элемента. [5]
Металлические свойства элементов возрастают справа налево по периодам и сверху вниз по группам. [6]
Металлические свойства элементов II Б - группы и основные свойства их оксидов и гидроксидов усиливаются от цинка к ртути: если оксид цинка ZnO обладает ярко выраженной амфотерностью, то у CdO она практически отсутствует, a HgO проявляет только основные свойства. [7]
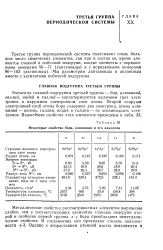 |
Некоторые свойства бора, алюминия и его аналогов. [8] |
Металлические свойства рассм-атриваемых элементов выражены слабее, чем у соответствующих элементов главных подгрупп второй и особенно первой группы, а у бора преобладают неметаллические свойства. [9]
 |
Свойства элементов подгруппы бора. [10] |
Металлические свойства элементов подгруппы бора выражены значительно слабее, чем у элементов подгруппы бериллия. [11]
Металлические свойства элементов подгруппы бора выражены значительно слабее, чем у элементов подгруппы бериллия. Так, элемент бор, который в периоде расположен между бериллием и углеродом, относится к элементам-неметаллам. Внутри подгруппы с возрастанием заряда ядра энергия ионизации атомов уменьшается и металлические свойства элементов усиливаются. Алюминий - уже металл, но не типичный. Его гидроксид обладает амфотерными свойствами. У таллия более сильно выражены металлические свойства, а в степени окисления 1 сн близок к элементам-металлам подгруппы лития. [12]
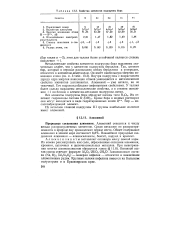 |
Свойства элементов подгруппы бора. [13] |
Металлические свойства элементов подгруппы бора выражены значительно слабее, чем у элементов подгруппы бериллия. Так, элемент бор, который в периоде расположен между бериллием и углеродом, относится к элементам-неметаллам. Внутри подгруппы с возрастанием заряда ядра энергия ионизации атомов уменьшается и металлические свойства элементов усиливаются. Алюминий - уже металл, но не типичный. Его гидроксид обладает амфотерными свойствами. У таллия более сильно выражены металлические свойства, а в степени окисления 1 он близок к элементам-металлам подгруппы лития. [14]
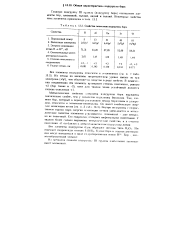 |
Свойства элементов подгруппы бора. [15] |
Страницы: 1 2 3 4