Основное свойство - гидроксид
Cтраница 2
Гидроксиды элементов подгруппы ПА Э ( ОН) 2 - более слабые основания, чем гидроксиды щелочных металлов. Основные свойства гидроксидов увеличиваются от Be ( ОН): к Ва ( ОН) 2; Ве ( ОН): и Mg ( OH) j - - слабые основания, Ва ( ОН) j - щелочь. [16]
 |
Свойства элементов II1A группы. [17] |
Гидроксиды элементов IIIA группы мало растворимы в воде. По сравнению с соответствующими соединениями элементов НА группы основные свойства гидроксидов элементов IIIA группы выражены в меньшей степени. [18]
Для Fe, Co и Ni характерны степени окисления 2 и 3; при переходе от F - e к Ni соединения со степенью окисления 3 становятся менее устойчивыми. В соответствии с небольшим уменьшением радиусов ионов при переходе от Fe к Ni основные свойства гидроксидов ослабевают. ОН) 2 являются неамфотер-ными основаниями, Э ( ОН) 3 - очень слабыми основаниями со слабо выраженными амфотерными свойствами. Соединения Fe2 являются восстановителями средней силы. В ряду Fe 2 - Со 2 - Ni 2 падает восстановительная способность. В ряду Fe 3 - Со 3 - Ni 3 возрастает окислительная способность. [19]
Для Fe, Co и Ni характерны степени окисления 2 и 3; при переходе от Fe к Ni соединения со степенью окисления 3 становятся менее устойчивыми. В соответствии с небольшим уменьшением радиусов ионов при переходе от Fe к Ni основные свойства гидроксидов ослабевают. ОН) 2 являются неамфотерными основаниями, Э ( ОН) 3 - очень слабыми основаниями с весьма слабо выраженными амфотерны-ми свойствами. Соединения Fe2 являются восстановителями средней силы. В ряду Fe 2 - Со 2 - Ni z падает восстановительная v способность. В ряду Ре 3 - Со 3 - № 3 возрастает окислительная способность. [20]
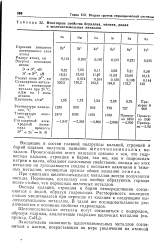 |
Некоторые свойства бернлляя, магния, радия и щелочноземельных металлов. [21] |
Оксиды кальция, стронция и бария непосредственно соединяются с водой, образуя гидроксиды. Растворимость последних сильно увеличивается при переходе от кальция к следующим щелочноземельным металлам. В такой же последовательности увеличиваются и основные свойства гидроксидов. [22]
Оксиды кальция, стронция и бария непосредственно соединяются с водой, образуя гидроксиды. Растворимость последних сильно увеличивается при переходе от кальция: к следующим щелочноземельным металлам. В такой же1 последовательности увеличиваются я основные свойства гидроксидов. [23]
Оксиды кальция, стронция и бария непосредственно соединяются с водой, образуя гидроксиды. Растворимость последних сильно увеличивается при переходе от кальция к следующим щелочноземельным металлам. В такой же последовательности увеличиваются и основные свойства гидроксидов. [24]
Оксиды кальция, стронция и бария непосредственно соеди няются с водой, образуя гидроксиды. Растворимость последних сильно увеличивается при переходе от кальция к следующим щелочноземельным металлам. В такой же последовательности увеличиваются и основные свойства гидроксидов. [25]
Оксиды кальция, стронция и бария непосредственно соединяются с водой, образуя гидроксиды. Растворимость последних сильно увеличивается при переходе от кальция к следующим щелочноземельным металлам. В такой же последовательности увеличиваются и основные свойства гидроксидов. [26]
Ион бериллия обладает меньшим радиусом, чем ионы других элементов II группы и создает поле большей напряженности. Поэтому Be ( ОН) г и ВеО обладают амфотерными свойствами. Однако как кислые, так и основные свойства гидроксида бериллия выражены слабо. [27]
Они имеют законченные 8-электронные внешние слои. Химическая активность их возрастает от кальция к барию. В таком же направлении изменяются и другие свойства, например растворимость солей, основные свойства гидроксидов и др. Ионы этих элементов в водных растворах бесцветны. [28]
Осадки разделите в две пробирки и в одну из них прилейте раствор кислоты ( азотной, соляной или серной), а в другую - концентрированный раствор щелочи. Как изменяются основные свойства гидроксидов при переходе от церия к лютецию. [29]
К третьей группе относятся катионы металлов бария, стронция, кальция. Они имеют законченные 8-электронные внешние слои. Химическая активность их возрастает от кальция к барию. В таком же направлении изменяются и другие свойства, например растворимость солей, основные свойства гидроксидов и др. Ионы этих элементов в водных растворах бесцветны. [30]
Страницы: 1 2 3