Связь - электрон
Cтраница 2
Энергия связи электрона - минимальная энергия, необходимая для удаления из атома электрона, находящегося в данном состоянии. [16]
Энергии связи электронов М -, L - и Л - - оболочек мышьяка равны 0 2, 1 5 и 11 9 кэв соответственно. [17]
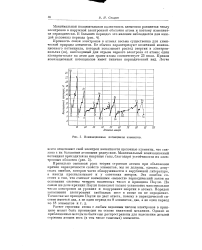 |
Ионизационные потенциалы элементов. [18] |
Прочность связи электронов в атомах весьма существенна для химической природы элементов. Ее обычно характеризуют величиной ионизационного потенциала, который показывает расход энергии в электрон-вольтах ( эв), необходимый для отрыва первого электрона от атома; один электрон-вольт на атом для грамм-атома соответствует 23 ккал. Кривая ионизационных потенциалов имеет типично периодический вид. [19]
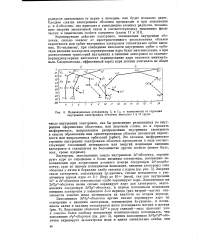 |
Ионизационные потенциалы 1г и / п в зависимости от строения внутренних электронных оболочек металлов I и II групп. [20] |
Энергия связи электронов, заполняющих 2р - уровень, сильно повышается с увеличением заряда ядра от 5 ( бор) до 10 ( неон), так как внутренние Is2 - и 252-оболочки относительно слабо экранируют ядро. Заполненная же 2я22рв - оболочка неона сильно экранирует ядро для электронов, заполняющих следующую 3 23р6 - оболочку, и первые потенциалы ионизации внешних электронов у элементов 3-го периода ( ряд натрий-аргон) оказываются заметно ниже потенциалов их аналогов во втором периоде. [21]
Энергия связи электрона и дырки равна как минимум ширине запрещенной зоны - энергетической щели между заполненной и свободной зонами диэлектрика. Эта ширина для диэлектриков достигает нескольких электрон-вольт. Поскольку 1 эВ равен 1 6 - 10 - у Дж, а постоянная Больцмана К 1 38 - 10 - 23 Дж / К, то легко подсчитать, что 1 эВ соответствует температуре, примерно равной 104 К. [22]
Энергии связи электронов 5 / -, Qd -, 7з - оболочек, участвующих в оптических переходах атомов урана и других тяжелых элементов, имеют очень близкие значения, а сам атом урана обладает низким ионизационным потенциалом. Спектр урана, как и других трансурановых элементов, является чрезвычайно сложным. В нем вместе с линиями нейтральных атомов присутствуют линии однократноио-низированных атомов, поэтому спектр урана представляет собой сплошную сетку линий, расположенных на фоне интенсивного непрерывного спектра. В связи с этим обычные методы спектрального анализа не могут применяться для успешного определения малых количеств примесей в уране. [23]
Энергии связи электронов 5 / -, Ы -, 7з - оболочек, участвующих в оптических переходах атомов урана и других тяжелых элементов, имеют очень близкие значения, а сам атом урана обладает низким ионизационным потенциалом. Спектр урана, как и других трансурановых элементов, является чрезвычайно сложным. В нем вместе с линиями нейтральных атомов присутствуют линии однократноио-низированных атомов, поэтому спектр урана представляет собой сплошную сетку линий, расположенных на фоне интенсивного непрерывного спектра. В связи с этим обычные методы спектрального анализа не могут применяться для успешного определения малых количеств примесей в уране. [24]
Энергией связи банного электрона в атоме называют количество энергии, необходимое для отделения его от атома. [25]
Прочность связи электронов внешнего слоя с ядром увеличивается. [26]
Прочность связи электронов внешнего слоя с ядром уменьшается. [27]
Конечно, связь электрона с А или с В не изменяет величины энергии; поэтому можно считать, что электрон может свободно переходить от одного ядра к другому. [28]
Характеризует прочность связи электрона в атомной системе. ИОНИЗАЦИЯ, превращение атомов или молекул в положит, ионы в результате отрыва одного или неск. Энергия, необходимая для отрыва электрона, наз. Нейтральные атомы и молекулы могут в особых случаях присоединять электроны, образуя отрицат. [29]
Значения энергии связи электронов табулированы, что позволяет проводить качеств, анализ. [30]
Страницы: 1 2 3 4