Связь - электрон
Cтраница 3
Мерой прочности связи электронов в атомах является величина энергии ионизации, или ионизационного потенциала ( гл. Очевидно, что восстановительная способность металлов связана с величиной энергии ионизации их атомов. Наименьшие значения ионизационного потенциала у щелочных металлов, которые и являются самыми энергичными восстановителями. [31]
Однако энергия связи электрона зависит и от внешнего электростатического потенциала. [32]
Если энергия связи электрона меньше, чем вершина потенциального барьера ( рис. 1), то ионизация может происходить за счет туннельного просачивания электрона через барьер из связанного в свободное состояние - это так называемый туннельный эффект. [33]
Значения энергии связи электронов табулированы, что позволяет проводить качеств, анализ. [34]
Мерой прочности связи электрона в атоме может служить потенциал ионизации атома ( см. гл. [35]
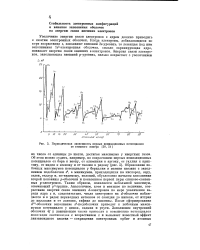 |
Периодическая зависимость первых ионизационных потенциалов от атомного номера. [36] |
Увеличение энергии связи электронов с ядром должно приводить к сжатию электронных оболочек. Когда электроны, добавляющиеся по мере возрастания z, заполняют внешний 2-уровень, то лежащая под ним заполненная 1 2-электронная оболочка, сильно экранирующая ядро, понижает энергию связи внешних s - электронов. [37]
Уменьшению энергии связи электронов с ядром, что способствует образованию катионов. [38]
Характеризует прочность связи электрона в атомной системе. ИОНИЗАЦИЯ, превращение атомов или молекул в положит, ионы в результате отрыва одного или неск. Энергия, необходимая для отрыва электрона, наз. Нейтральные атомы и молекулы могут в особых случаях присоединять электроны, образуя отрицат. [39]
Однако энергия связи электронов первых подуровней данной оболочки может быть большей, чем энергия электронов последних подуровней предыдущей оболочки. Поэтому 19 - й электрон атома калия и 20 - й электрон атома кальция не начинают постройки Sd-подуровня, а занимают 45-положение, так как это соответствует большей энергии связи их в атоме. Таким образом, последовательность в образовании электронами оболочек атома в этом случае нарушается. [40]
Однако энергия связи электронов первых подгрупп данной оболочки может быть большей, чем энергия электронов последних подгрупп предыдущей оболочки. Поэтому 19 - й электрон атома калия и 20 - й электрон атома кальция не начинают постройки Sd-подгруппы, а занимают 4 - 5-положение, так как это соответствует большей энергии связи их в атоме. Таким образом, последовательность в образовании электронами оболочек атома в этом случае нарушается. И только когда наиболее выгодная в энергетическом отношении s - подгруппа четвертой оболочки достроена, следующие электроны в атомах скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля и меди окончательно достраивают третью оболочку. [41]
Она обусловлена связью электронов с электрическими и магнитными моментами ядра. В этой главе мы установим вид взаимодействий, описывающих такую связь. Начнем с наиболее простых электростатических взаимодействий, хотя практически они и менее важны. [42]
В окрашенных соединениях связь электронов с ядром ослаблена, вследствие чего энергия лучей видимого света оказывается достаточной для возбуждения электронов. Ниже будут подробно рассмотрены причины, обусловливающие повышенную подвижность электронов и перераспределение плотности электронного облака в молекулах красителей. [43]
В таких кристаллах связь электронов с ионами слабая. [44]
В окрашенных соединениях связь электронов с ядром ослаблена, вследствие чего энергия лучей видимого света оказывается достаточной для перемещения электронов, почему и может происходить поглощение видимого света. [45]
Страницы: 1 2 3 4