Связь - электрон
Cтраница 4
 |
Известные изотопы некоторых элементов. [46] |
Разница в энергии связи электронов 5 / - и G / i-подуровней в атомах этих элементов весьма незначительна, в особенности для Th и Ра. На рис. 8 показаны сравнительные значения энергии, необходимой для отделения наиболее легко удаляемого электрона в атомах элементов этих подуровней. [47]
Вследствие максимальной энергии связи электронов с ядрами посредине между ядрами ( в точке касания жестких шаров) в об-ласт ЬнЛерекрытия стягиваются электроны из периферийных участков s - орбиталей, что ведет к дальнейшему повышению плотности s - состояний в зонах перекрытия. [48]
Разница в энергии связи электронов 5 / - и Gd-подуровней в атомах этих элементов весьма незначительна, в особенности для Th и Ра. На рис. 8 показаны сравнительные значения энергии, необходимой для отделения наиболее легко удаляемого электрона в атомах элементов этих подуровней. [49]
Влияние на прочность связи электронов с ядром оказывает также взаимное отталкивание электронов одного и того же слоя и в особенности одной и той же орбитали. [50]
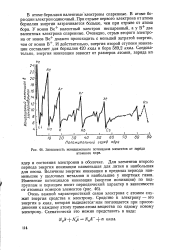 |
Зависимость ионизационного потенциала элементов от заряда. [51] |
Очень важной характеристикой связи электрона с атомом служит энергия сродства к электрону. Сродство к электрону - это энергия в ккал, которая выделяется или поглощается при присоединении к каждому атому грамм-атома вещества по одному новому электрону. [52]
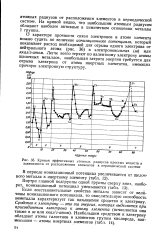 |
Кривая эффективных атомных радиусов простых веществ в зависимости от расположения элементов в периодической системе. [53] |
О характере прочности связи электронов в атоме элемента можно судить по величине ионизационного потенциала, который показывает расход необходимой для отрыва одного электрона от нейтрального атома ( рис. 36) в электроновольтах ( эв) или ккал / г-атом. Легче всего теряют по валентному электрону атомы щелочных металлов, наибольшая затрата энергии требуется для отрыва электрона от атома инертных элементов, имеющих прочную электронную структуру. [54]
Чем меньше энергия связи электронов с ядром, тем проще отрыв их от атома, тем легче они образуют обобществленные электроны. [55]
Страницы: 1 2 3 4