Делокализованная связь
Cтраница 1
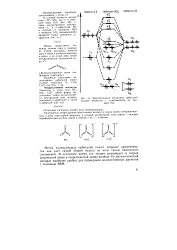 |
Энергетическая диаграмма орбиталей угловой молекулы с л-связыванием на примере SO2. [1] |
Делокализованная связь изображена пунктиром. [2]
Пунктиром показана делокализованная связь, причем для первых трех частиц это я-связь, а для Хер2 - 0-связь. [3]
Для соединений с делокализованными связями используются те же два главных общих метода приближенного решения уравнения Шредингера, которые рассматривались в гл. В методе валентных схем молекулу изображают несколькими возможными структурами Льюиса ( называемыми каноническими формами) и считают, что она представляет собой среднее между весами, или вкладами, этих структур, каждой из которых отвечает своя волновая функция г з в уравнении ( 2) ( см. гл. [4]
 |
Направления перекрывания атомных d - орбиталей при образовании 8-связей. [5] |
Другими примерами соединений с делокализованными связями служат молекула озона О3, бензола ( см. гл. [6]
Это объясняется увеличением в сульфидах доли делокализованной связи. [7]
Электронная структура некоторых карбонильных кластеров в приближении делокализованных связей М - м была расомотрена в качественной форме Далем, Альбано и Льюисом ( цит. Недостаточность использованного этими авторами подхода состоит не только в его качественной форме, но и в больней степени в том, что играющие первостепенную роль в формировании природы карбонильных кластеров дативные it - связи м-со практически не учитываются. [8]
Наиб, существенной особенностью сопряженных систем с делокализованными связями является их повыш. В сопряженных системах правилам аддитивности не подчиняются также параметры ИК спектров, величины дипольных моментов и поляризуемости, диамагнитной восприимчивости и др. В этих случаях при расчете разл. [9]
 |
Разбиение объема молекулы ABCD на лоджии. [10] |
В этом случае мы должны ввести концепцию р-электропной делокализованной связи, размазанной по q атомным остовам. [11]
В этом случае мы должны ввести концепцию р-электронной делокализованной связи, размазанной по q атомным остовам. [12]
В ряду F-О - N-С повышается способность к образованию соединений с делокализованной связью, вплоть до металлической. Металлическими являются карбиды ( - элементов IV-VIII групп. Карбиды этого типа представляют собой соединения включения; в них атомы углерода занимают октаэдрические пустоты в плотноупакованных структурах атомов металлов. Металлические карбиды весьма разнообразны. Эти карбиды проявляют металлические признаки: металлический блеск, высокую электрическую проводимость, уменьшающуюся с повышением температуры, легкость образования твердых растворов с металлами и др. Состав карбидов rf - элементов изменяется в широких пределах. [13]
В заключение следует отметить, что хотя реальная структура соединений с делокализованными связями не соответствует в точности ни одной резонансной структуре, но при реакции молекулы этих соединений ведут себя так, как если бы в момент столкновения с частицей реагента они обладали определенной резонансной структурой. [14]
 |
Три связывающие орбитали 3-метилен - 1 4-пентадиена ( 9. [15] |
Страницы: 1 2 3