Аксиальная связь
Cтраница 2
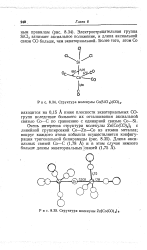 |
Структура молекулы Co ( SiCl3 ( CO4.| Структура молекулы Zn [ Co ( CO 4 ] 2. [16] |
Электроотрицательная группа SiCl3 занимает аксиальное положение, и длина аксиальной связи СО больше, чем экваториальной. [17]
Согласно этой теории, потенциальные барьеры не являются свойством самой аксиальной связи, но возникают в результате обменного взаимодействия электронов, участвующих в других связях, образованных двумя атомами. Иными словами, потенциальные барьеры возникают в результате перекрывания орбит этих связей. [18]
Этот и лид реагирует с циклогексаноном, давая эпоксид с аксиальной связью С - О. [19]
Однако в молекуле НМп ( СО) 5 по данным рентгенострук-турного анализа [85] аксиальная связь Мп - С длиной 1 821 А, если и укорочена по сравнению со средней экваториальной 1 836 А, то очень незначительно, а длины связей С - О не различаются. [20]
Когда в узлах сочленения циклов имеются две аксиальные связи, то система с аксиальными связями в 1 2 - и 1 4-положении по отношению друг к другу стабильнее системы с аксиальными связями в 1 3-положении. В последней существует сильное взаимодействие 1 3-диаксиальных метиленовых групп ( ср. [21]
Наибольшее отталкивание от электронных пар наименее электроотрицательных заместителей приводит к отклонению от этих заместителей аксиальных связей. [22]
Почти во всех случаях атом металла расположен на значительном расстоянии от основания пирамиды, и аксиальная связь длиннее, чем связи, лежащие в основании пирамиды. Исключения представляют комплексы Ni ( DEAS) 2, у которого аксиальная связь немного короче связей, лежащих в основании, что пока трудно объяснить, и бис - ( ацетилацетонато) оксованадий ( 1У) с очень короткой аксиальной связью. [23]
По мере увеличения числа метильных групп все длины связей растут, увеличивается и отношение длины аксиальной связи к длине экваториальной. [24]
Модель Рандла не требует привлечения d - орбиталей центрального атома, а использует для образования аксиальных связей его Зр-орбитали, что определяет большую длину и полярность аксиальных связей по сравнению с экваториальными. Схема Рандла находится в хорошем согласии с данными Бартела и Хансен; 1 4, однако она не ведет к прямому предсказанию величин параметров связей, что обусловлено произвольным допущением о полном использовании Ss-орбиталей в экваториальных связях. [25]
Теория приводит к общей оценке, согласно которой величина барьера составляет около 4 / от энергии аксиальной связи в том случае, когда у каждого из двух атомов имеется по три взаимодействующих связи. Теория Полинга представляется весьма перспективной. [26]
На основе изменений длин связей Fe-N, наблюдающихся при изменении спинового состояния, можно ожидать аналогичные эффекты для аксиальной связи Fe - - N, образуемой с проксимальным имидазольным кольцом ( Fe-Мимидазол) - Однако природа аксиальной связи Fe-Мимадазол в гемовых комплексах при изменении спинового состояния до сих пор не ясна. [27]
Последняя реакция не протекает, так как в результате ее кольцо А должно быть сочленено с кольцом В двумя аксиальными связями, что практически невозможно. [28]
В нем атом иода окружают семь электронных пар, простейшим симметричным расположением которых является пентагональная бипирамида ( 94) с двумя аксиальными связями I-F, оставшиеся пять связей равномерно распределены в плоскости ху. Результаты исследований показывают, что молекула имеет строение, достаточно близкое к идеальному, но в группе IPs наблюдается небольшое отклонение от плоского расположения атомов. [29]
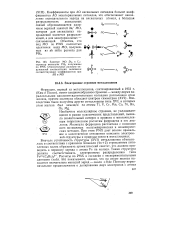 |
Занятые МО D3h и C4v структур молекулы PHs, полученные по РМХ. Относительные размеры окружностей соответствуют величинам соответствующих коэффициентов при АО в МО. [30] |
Страницы: 1 2 3 4