Слабая водородная связь
Cтраница 2
Но этим не ограничивается роль слабых водородных связей в процессах жизнедеятельности. Именно благодаря этим связям происходит точное копирование молекулы ДНК, передающей из поколения в поколение всю генетическую информацию; водородные связи определяют специфичность действия многих лекарственных препаратов; ответственны они за вкусовые ощущения, и за способность наших мышц сокращаться... Одним словом, в живой природе атом водорода действительно незаменим. [16]
 |
Схема вторичной структуры белковой молекулы.| Схема третичной структуры белковой молекулы. [17] |
Вторичная и третичная структуры обусловлены слабыми водородными связями и устойчивы только в определенных условиях. Например, растворимый в воде белок при умеренном нагревании или изменении кислотности становится нерастворимым и свертывается. [18]
Отсюда следует, что при слабых водородных связях, чаще всего образующихся в кристаллогидратах и водных растворах, TQH увеличивается обычно на 0 01 - 0 02 А, а иногда и до 0 03 А. [19]
Можно полагать, что в очень слабых водородных связях равновесная длина А - Н практически остается такой же, как и в свободной молекуле. [20]
Общей теории уширения полос под действием слабой водородной связи пока не существует. Однако тот факт, что уширение VQH-ПОЛОС имеет место не только тогда, когда расстояние до первого колебательного уровня оказывается больше энергии диссоциации Н - связи, но и когда оно меньше ( внутримолекулярные Н - связи), показывает, что если преддиссоциация и оказывает влияние на ширину полос, то не определяющее. [21]
Хорошо известно, что сера образует слабую водородную связь. Поэтому кажется вероятнее всего, что G % связывается со спиртовым кислородом сложноэфирной группы путем образования водородного мостика, но в случае тиоловых эфиров это должно происходить в значительно меньшей степени. Связывание G2 способствует повышению скорости гидролиза, так как, когда G2 становится инактивированным в результате повышения рН, скорость убывает. Ввиду того что рКь - 9, можно предположить, что фенольный гидроксил тирозина выполняет функции G2, но не исключены и другие возможности. [22]
К первой группе относят растворители со слабыми водородными связями, в которых межмолекулярные силы имеют дисперсионный или слабополярный характер; ко второй группе - растворители с водородными связями средней силы, в которых проявляется взаимодействие между полярными группами; к третьей группе - растворители с сильными водородными связями, имеющими главным образом характер водородных мостиков. [23]
Следует отметить, что для льда характерна очень слабая водородная связь атомов, причем их подвижность резко уменьшается с понижением температуры, что и обусловливает упрочнение структуры льда. [24]
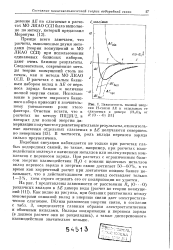 |
Зависимость полной энер гии Н - связи АЕ и отдельных ее слагаемых в димере ( Н20 г от R ( О О [ И ]. [25] |
Подобная ситуация наблюдается не только при расчетах слабых водородных связей, но также, например, при расчетах взаимодействия молекул с катионами металлов или молекулярных комплексов с переносом заряда. [26]
 |
Зависимость полной энергии Н - связи Д. и отдельных ее слагаемых в дилере ( Нс. 0 г от R ( О. - - О. [27] |
Подобная ситуация наблюдается не только при расчетах слабых водородных связей, но также, например, при расчетах взаимодействия молекул с катионами металлов или молекулярных комплексов с переносом заряда. При расчетах с ограниченным базисом энергии взаимодействия Н20 с ионами щелочных металлов: вклад переноса заряда в энергию связи достигает 50 - 60 %, в то. [28]
В первом случае остов аддуктов образуется посредством сравнительно слабых водородных связей, во втором - при помощи прочных ковалентных связей. [29]
Страницы: 1 2 3 4
