Слабая водородная связь
Cтраница 4
Специфическое взаимодействие кислоты А с молекулой S как с основанием ( очень слабая водородная связь) отнюдь не исключается. [46]
При ЛрК - 9 0 между донором я акцептором протона образуется липа слабая водородная связь, а при ДрК 4 5 И - - ДЯ 9 5 ккад / моль осуществляется полный перенос протона от молекулы кислоты к молекуле основания, и появляются продукты при -, соединения ионного характера. [47]
 |
Зависимость концентрации соли [ ТЛАНХ ] 0рг от [ ТЛА ] 0рг - анх Для хлороформа. Состав обеих фаз определен титрованием и измерением рН ( 10. [48] |
Ассоциация ионов не является чисто электростатическим процессом, но может включать образование слабой водородной связи между аммониевым катионом и анионом. Последнее взаимодействие тем сильнее, чем меньше анион и чем он более основен. [49]
Измерения, наблюдающиеся в контуре полосы гидроксильных групп, указывают на образование слабой водородной связи. [50]
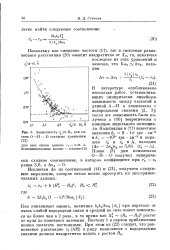 |
Зависимость г й от До для систем О - Н -. - О согласно уравнению ( 22. [51] |
Как показывает оценка, величина k / Пкч k при переходе от очень слабой водородной связи и средней по силе может измениться не более чем в 2 раза, в то время как Xl - ( R0 - о) 2 растет от нуля до конечного значения. [52]
Сероводород в конденсированном состоянии, по-видимому, в некоторой мере ассоциирован посредством сравнительно слабых водородных связей SH - - - S. Существование межмолекулярных водородных связей SH - - - SP доказано Ал-фордом и др. [301--303] по инфракрасным спектрам. В спектрах разбавленных растворов фосфородитиокислот [301], фосфинодитиокислот [302] и фосфоротетратиокислот [303] в четыреххлористом углероде наблюдается увеличение частоты VSH на 110 - 140 см-г по сравнению с этой частотой в спектрах соответствующих чистых жидкостей. [53]
Белый, в кристаллической решетке - молекулы NH3 и Н2О, связанные слабой водородной связью H3N - НОН. Термически неустойчив, полностью разлагается при кипячении раствора. Проявляет восстановительные свойства ( за счет N-IH) в концентрированном растворе. Вступает в реакции двойного обмена и комплексообразования. Применяется для создания слабощелочной среды в растворе, осаждения амфотерных гидроксидов. [54]
Путем сравнения вычисленной величины 7Уд; с экспериментально найденной можно было доказать существование слабой водородной связи ( или вообще пространственного взаимодействия) даже у производных с вицинальными гидроксильными группами, а также у производных с гидро-ксилыюй и карбоксильной группами, находящимися у одного атома. [55]
Страницы: 1 2 3 4