Сильная водородная связь
Cтраница 1
Сильная водородная связь не проявляется в биологических системах. Что же касается слабой водородной связи, то она имеет решающее значение во всех живых организмах. [1]
Сильная водородная связь между спиртовой группой и молекулой растворителя может вызвать сдвиг положения линии поглощения гид-роксила в сторону низких напряженностей поля. Кроме того, замедляется скорость химического обмена, так что можно наблюдать спин-спиновое взаимодействие гидроксильного протона с протонами, которые связаны с соседними атомами. [2]
Образование сильных водородных связей объясняет также следующий факт, вытекающий из рис. 88, г [ разд. [3]
При очень сильных водородных связях в спектрах наблюдаются некоторые интересные изменения, которые полностью не объяснены. Типичные явления, которые обнаруживаются при этом, состоят в появлении нескольких широких полос в области частот выше 2000 CMTV или даже в отсутствии каких-либо полос в области выше 1600 см-1, но в значительном увеличении фона поглощения во всей низкочастотной области. [4]
Вследствие образования сильных водородных связей характерные для паров воды вращательные полосы в спектрах жидкой воды не проявляются. [5]
Классический пример сильных водородных связей между молекулами дает вода. [6]
Ионы с сильными водородными связями и каталитическое действие растворов кислот и оснований: Автореф. [7]
Это объясняется образованием сильных водородных связей между двумя кислотными остатками, что характерно вообще для сред, резко отличных от воды ( гл. [8]
Кислоты вследствие существования сильных водородных связей между карбоксильными группами часто образуют термотропные жидкие кристаллы. Необходимым условием является присоединение СООН-группы к жесткой, обычно ароматической части. Алифатические карбоксильные соединения, за исключением, возможно, алкановых кислот, содержащих сопряженные двойные связи, являются изотропными выше своих температур плавления. [9]
Хотя большинство исследований исключительно сильных водородных связей этого типа относятся к системам ОН - - О или иногда к ОН - - N, совершенно аналогичные результаты получаются в случае связей NH - - О и NH - - N при условии, что обеспечивается резонансная структура. Особенно благоприятным оказывается случай, когда две пары водородных связей расположены симметрично, так что перекрестный перенос протона по обеим связям приводит к очень малому или нулевому изменению энергии. Это обеспечивается, когда имеются две потенциальные ямы равной глубины, хотя при этом ничего неизвестно о высоте барьера. Примеры некоторых водородных связей NH - - О значительной силы, возникающих при таких условиях, приведены Беллами и Рогашем [18], а также Рейном и Харрисом [161], которые исследовали ассоциацию гуанидина с цитозином. Полоса С в спектре даже более интенсивна, чем полосы А и В, но скорее всего она обусловлена колебанием связи ОН - - О. [10]
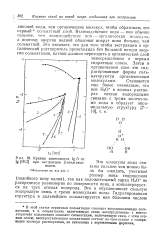 |
Кривые зависимости lg D от. [11] |
Это и обусловливает сильную водородную связь с тремя молекулами воды. [12]
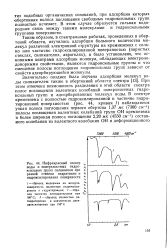 |
Инфракрасный спектр воды и поверхностных гидро. [13] |
В этом случае образуется сильная водородная связь между такими молекулами и гидроксильными группами поверхности. [14]
Способность растворителя к образованию сильных водородных связей с кислотой или основанием также оказывает значительное влияние на константу диссоциации ( см. обсуждение вопроса о роли сольватации, стр. [15]
Страницы: 1 2 3 4