Сильная водородная связь
Cтраница 2
Действие ДМСО объясняется образованием сильных водородных связей гидроксильных групп с молекулами растворителя. [16]
При образовании комплексов с сильной водородной связью значительно изменяется конфигурация молекул. Потенциальная энергия протона имеет один сравнительно плоский минимум, расположенный примерно в центре связи. Поэтому протон легко смещается. Легкая смещаемость протона под влиянием внешнего поля обусловливает большое значение поляризуемости комплекса. [17]
Дж / моль объясняется сильными водородными связями. [18]
Описаны многие системы с сильными водородными связями. Хаджи [125, 149-153] представил примеры различных типов связей вместе с данными о смещениях частот и расстояниях Х - - Y в тех случаях, когда эти величины известны. Шеппард [154] и Рыс-кин [155] также исследовали ряд таких связей; кроме того, имеются многочисленные исследования индивидуальных соединений, в частности работы Спикмена [156], рассмотревшего системы с симметричными связями О - - Н - - О. [19]
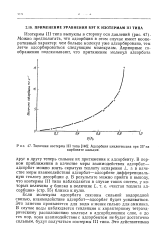 |
Типичная изотерма III типа. Адсорбция циклогексана при 25 на. [20] |
Если молекулы адсорбата связаны сильной водородной связью, взаимодействие адсорбат-адсорбат будет усиливаться. Это заметно проявляется для воды и менее сильно для аммиака. В случае воды наблюдается тенденция к характерному тетраэд-рическому расположению молекул в адсорбционном слое, а до тех пор, пока взаимодействие с адсорбентом не будет достаточно сильным, будут получаться изотермы III типа. [21]
Карбоксильная группа вовлекается в образование сильной водородной связи между двумя молекулами. [22]
Неплоская форма молекул обусловлена образованием сильных водородных связей, что в некоторых оксалатах влечет за собой небольшое изменение длины связей С-О. [23]
Так, свойство глицерина образовывать сильную водородную связь с водой позволяет использовать его для разделения смесей, содержащих воду. Разделение первичных, вторичных и третичных аминов на полиэтиленоксиде объясняется различной способностью аминов образовывать водородные связи с неподвижной фазой. Доля водородной связи в общей энергии взаимодействия веществ уменьшается по мере роста их молекулярной массы. Фторзамещенные силоксаны обеспечивают преимущественное удерживание сорбатов с карбонильными группами ( альдегидов и кетонов) по сравнению с сорбатами, имеющими карбоксильные группы. [24]
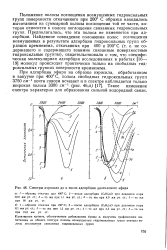 |
Спектры аэросила до и после адсорбции диэтилового эфира. [25] |
Такое изменение спектра характерно для образования сильной водородной связи. [26]
Как упоминалось выше, в случае сильных водородных связей наблюдается большой изотопический эффект для расстояния А - - В, который невозможно объяснить на основе модели с одной потенциальной ямой, применимой для слабых связей. Весьма вероятно, что величина этого эффекта существенно зависит от формы потенциальной кривой для протона и становится значительной при появлении двойного минимума. Если окажется, что это действительно так, то наличие сильного изотопического эффекта для R будет веским аргументом в пользу гипотезы о том, что потенциальная кривая имеет два минимума. [27]
Образование ионной пары должно сопровождаться возникновением сильной водородной связи, при которой происходит простой и очень быстрый перенос протона и образование Fe ( H90) 5OH2, НХ. Наличие гидроксогруппы в комплексе должно увеличивать скорость реакции. [28]
Как правило, ионные пары с сильной водородной связью проявляют относительно слабую тенденцию к полимеризации. Степень ассоциации пикратов три - - бутил-аммония и триизоамиламмония в бензоле равна только 1 01 при формальной концентрации соли 0 001-и воз-растает лишь до 2 2 при концентрации 0 3 [11] ( ср. [29]
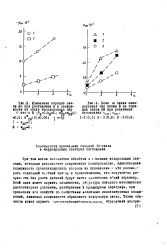 |
В лая. ш числа неподеленных пар атома В на порядок связи НВ при различных отношениях кдн. кнв. [30] |
Страницы: 1 2 3 4