Вычисленное экспериментальное значение
Cтраница 3
Показатель степени г подбирается с таким расчетом, чтобы величина расхождения между вычисленными и экспериментальными значениями X смеси была наименьшей. [31]
Из результатов, приведенных в табл. 1 и 2, следует, что вычисленные и экспериментальные значения коэффициентов распределения находятся в хорошем согласии. Это значит, что сведения о комплексообразо-вании различных ионов в водном растворе, полученные методом ионного обмена, соответствуют действительности и могут быть использованы для предсказания поведения металлов в экстракционных системах с трибу-тилфосфатом. По-видимому, нет оснований сомневаться, что использование различных данных о комплексообразовании будет успешным при описании всех экстракционных систем, в которых образуется один экстракционный комплекс. [32]
 |
Спектр ЭПР иона. [33] |
Аналогичные расчеты для изоэлектронных ионов V2 и Мп4 указывают на увеличивающуюся разницу между вычисленными и экспериментальными значениями - факторов с ростом номинального заряда иона. Таким образом, различие между евычисл и gaKcn связано с наличием ковалент-ной связи между ионом и лигандами. [34]
Конкретные расчеты, выполненные для алканов ( см. § 6), дают вполне удовлетворительную сходимость вычисленных и экспериментальных значений. [35]
Вычислить теоретически значения коэффициента / для многоатомных газов не представляется возможным, так как расхождения между теоретически вычисленными и экспериментальными значениями весьма велики. [36]
Если при теоретическом расчете спиновых плотностей сразу учитывается сверхсопряжение с протонами СН2 - групп [188, 189], то вычисленное и экспериментальное значения асн совпадают. [37]
Стерическим фактором этот коэффициент называется не потому, что только пространственные препятствия являются единственной причиной расхождения между вычисленными и экспериментальными значениями константы скорости. [38]
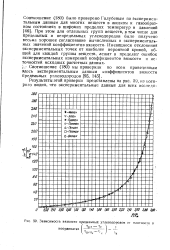 |
Зависимость вязкости предельных углеводородов от плотности в. [39] |
При этом для отдельных групп веществ, в том числе для предельных и непредельных углеводородов было получено весьма хорошее согласование вычисленных и экспериментальных значений коэффициентов вязкости. Имеющиеся отклонения экспериментальных точек от наиболее вероятной кривой, общей для каждой группы веществ, лежат в пределах ошибок экспериментальных измерений коэффициентов вязкости и неточностей исходных расчетных данных. [40]
Как видно из табл. 11, для стержнеобразных молекул N2, О2, С2Н4, СаНе, Ы2О и СО2 потенциал Кихара дает более удовлетворительное совпадение между вычисленными и экспериментальными значениями РДИсс -, чем потенциалы Леннард-Джонса 12 - 6 и 28 - 7, В дальнейших работах [36, 38] Нагата и Кобаяси, пользуясь известными экспериментальными значениями Рдисс. Кихара с достаточной надежностью, а затем вычислили для азота константы Лэнгмюра применительно к гид-ратной структуре I. Следует отметить, что вычисления констант Лэнгмюра проводились на основании двух моделей молекулы: линейной и стержнеобразной. [41]
Это не может, однако, являться полным объяснением, так как в случае веществ, для которых массопередача в жидкой фазе весьма мала, существует большое различие между вычисленными и экспериментальными значениями С. [42]
Обе величины ( у и х), входящие в выражение для Р ( х, у), известны из эксперимента, и поэтому не требуется введения каких-либо произвольных постоянных, Совпадение вычисленных и экспериментальных значений ( для смеси С6Н6 - С7Н8) следует признать удовлетворительным, если учесть сделанные при теоретическом анализе сильно упрощающие задачу предположения. [43]
Результаты расчетов для высоких давлений представлены в той же таблице 33, из которой видно, что вычисленные по формуле ( 164) данные занижены, при этом, чем больше давление, тем больше расхождение между вычисленными и экспериментальными значениями вязкости. [44]
Количественный метод определения констант гидролиза предложен Каспером ( цит. Вычисленные и экспериментальные значения первых констант гидролиза для большого числа трех - и четырехзарядных положительных ионов плутония, приведенные в обзорной статье Дж, Хайнд-мэна [7], подтверждают применимость метода Каспера. [45]
Страницы: 1 2 3 4