Чисто ковалентная связь
Cтраница 2
Как показали исследования Горди, вклад - электронов в константу eQq при образовании чисто ковалентной связи не меняется от атома к молекуле. [16]
Итак, как мы уже указывали выше, данная связь А-В является либо чисто ковалентной связью, либо она обладает дополнительной ионной резонансной энергией. [17]
Другой результат резонанса - уменьшение междуатомных расстояний по сравнению с теми, которые дает чисто ковалентная связь. При резонансе между связями разной кратности междуядерные расстояния имеют промежуточные значения. Такое уменьшение расстояния является прямым следствием увеличения энергии связи от резонанса. [18]
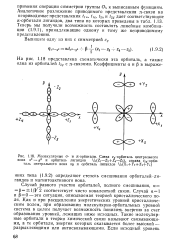 |
Молекулярные а - и я-орбитали. Слева ег-орбиталь центрального иона х2 - у2 и орбиталь лигандов lh ( Z - Z2 Z4 - Z5, справа таль центрального иона ху и орбиталь лигандов. [19] |
Случай равного участия орбиталей, полного смешивания, а Р 1 / К2 соответствует чисто ковалентной связи. [20]
Как известно, углерод занимает в таблице Менделеева особое положение, определяемое способностью к образованию чисто ковалентных связей за счет неспаренных электронов. На языке квантовой механики это означает чисто обменное взаимодействие между валентными электронами смежных С-атомов. Строго говоря, поляризация возникает уже в гетероцепных органических полимерах и может быть усилена или ослаблена за счет боковых радикалов. [21]
Проведенное выше рассмотрение характера связи в HF показывает, что не существует чисто ионных, как и чисто ковалентных связей. Не существует и принципиального различия между этими двумя типами связи - они лишь являются предельными случаями непрерывного ряда связей с различной полярностью. В рамках теории молекулярных орбиталей гораздо большее значение, чем оценка ионного характера связи, имеет близость энергетических уровней взаимодействующих орбиталей двух атомов. Эта степень близости уровней связана с электроотрицательностью атомов. [22]
Для описания соединения как чисто ковалентного следует, учитывая координацию атомов в кристалле, определить возможную конфигурацию чисто ковалентной связи. [23]
Стеклообразное состояние характеризуется искажением длин связей и углов, поэтому [100] стекла не могут образовываться из соединений с чисто ковалентными связями, для которых характерна направленность, а следовательно, и постоянство длин связей и углов. Вещества с чисто ионными или металлическими связями не дают стекол, так как для них не характерна направленность. Поэтому стекла образуются из вещества со смешанной связью: ионно-ковалентно. [24]
Под Wi и We подразумеваются не энергии решетки сосуществующих форм, а те энергии, которые имела бы решетка в случае чисто ионной или чисто ковалентной связи. [25]
Под H j и Wc подразумеваются не энергии решетки сосуществующих форм, а те энергии, которые имела бы решетка в случае чисто ионной или чисто ковалентной связи. [26]
Здесь нормальные алканы рассматриваются как эталонные неполярные вещества, молекулы которых не образуют водородных связей и содержат лишь - СН3 и - СНг - алкильные группы с чисто ковалентными связями. [27]
Здесь нормальные алканы рассматриваются как эталонные неполярные вещества, молекулы которых не образуют водородных связей и содержат лишь - СН3 и - СНу - алкильные группы с чисто ковалентными связями. [28]
Здесь нормальные алканы рассматриваются как эталонные неполярные вещества, молекулы которых не образуют водородных связей и содержат лишь - СН3 и - СНг - алкильные группы с чисто ковалентными связями. [29]
Бор характеризуется малым сродством к электрону и образует с металлами соединения преобладающего ковалентного характера, где атомы бора связаны друг с другом в пары, цепочки, гексагональные сетки и комплексы чисто ковалентными связями. [30]
Страницы: 1 2 3 4