Чисто ковалентная связь
Cтраница 3
Ковалентные расстояния вычислены по радиусам, данным в § 16.10, а не по приведенным в табл. 33, так как можно считать, что первые дают величины более близкие к радиусам, ожидаемым при чисто ковалентной связи. [31]
Алканы н-строения среди углеводородов являются наиболее простыми по молекулярному строению и имеют наибольшее число хорошо изученных гомологов, их молекулы составлены ( за исключением метана) только из ( СНз - ) и ( - СН2 - ) структурных составляющих с чисто ковалентными связями. [32]
Алканы н-строения среди углеводородов являются наиболее простыми по молекулярному строению и имеют наибольшее число хорошо изученных гомологов, их молекулы составлены ( за исключением метана) только из ( СНз - ) и ( - CHj - ) структурных составляющих с чисто ковалентными связями. В этой связи они рассматриваются как эталонные вещества, а остальные углеводороды и гетероорганические соединения - как производные н-алканов ( изо-апканы - как алкилалканы, нафтены - как алкилциклопентаиы или алкилцикло. [33]
В этих примерах полярность связей уменьшается; наиболее полярна ге-тероатомная связь He - Fe -, наименее полярна гетероатомная связь С19 - N6 ( разделение зарядов проведено по более точным данным XN 3 07 и Xci 2 83; см. Приложение 4), чисто ковалентная связь С1 - CI неполярна. [34]
Рассмотренная до сих пор картина связей предполагает, что: 1) связи являются чисто ковалентными и 2) порядки связей представляют собой целые числа. Чисто ковалентная связь соответствует равному обобществлению пар электронов, а целочисленный порядок связи означает, что пары электронов либо обобществлены полностью, либо не обобществлены совсем. Большинство реальных примеров нельзя описать удовлетворительно в рамках этих ограничений, и для них требуется описание, которое можно аппроксимировать с помощью соответствующим образом подобранных комбинаций таких простых волновых функций. [35]
Таким образом, описываемый метод основан на эмпирической формуле, выполняющейся лишь для некоторых простейших систем, распространяемой на сложные гетерогенные системы. Для чисто ковалентной связи эта специфика вообще не принимается во внимание. Таким образом, специфика влияния поверхности фактически трактуется как вклад ее ионного характера связи. [36]
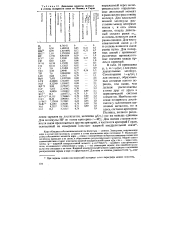 |
Дипольные моменты молекул в степень полярности связи по Полингу и Горди. [37] |
Для идеальной, ионной молекулы расстояние между центрами ионов ге и есть длина диполя, откуда дипольный момент равен еге, и степень ионности связи равна единице. Для чисто ковалентной связи ц 0 и степень ионности связи равна нулю. Для полярных связей У принимает различные промежуточные значения между нулем и единицей. [38]
Оба рассмотренных типа связи - ионная и ковалент-ная - представляют из себя два крайних случая. Чисто ионная или чисто ковалентная связь встречается сравнительно редко. Обычно в силу различной электроотрицательности атомов и их взаимного влияния электронное облако, образующее связь, как говорилось, всегда несколько смещено в сторону какого-либо одного из атомов. Это и делает связи полярными. Степень их полярности определяется разницей в электроотрицательности связываемых атомов. С уменьшением этой разницы связь по своему характеру все больше приближается к кова-лентной, и наоборот, с увеличением - к ионной. [39]
Чисто ионная связь и чисто ковалентная связь представляют собой предельный случай; реальная связь между двумя атомами не бывает ни чисто ионной, ни чисто ковалентной. Например, пространственная форма молекулы воды представляет собой угол, в вершине которого находится кислород. [40]
Предполагается, что энергия чисто ковалентной связи между А и В равна 1 / г [ Е ( А. Величина с зависит, очевидно, от различия в электрохимическом характере А и В, и, следовательно, и полярность связи и Д также зависят от этого различия. [41]
А - - Х) или Аб - Хб -, где X - более электроотрицательный атом, а 6 и б - означают частичные электрические заряды, возникшие на атомах в результате поляризации связи. Поляризованная связь может рассматриваться как резонансный гибрид чисто ковалентной связи с симметричным распределением электронной плотности и чисто ионной связи А Х -, где оба электрона полностью перешли к более электроотрицательному атому. На молекулярно-орбитальной картине, которая является дополнением к резонансному описанию, место повышенной электронной плотности указывается более интенсивной штриховкой. [42]
Коэффициент а относится к а-разрыхляющей, a PJ и р - соответственно к плоской и неплоской я-разрыхляющим орбиталям. Эти величины могут изменяться от 0 5 для чисто ковалентной связи до 1 0 для чисто ионной связи. [43]
Отметим, что чисто ионная и чисто ковалентная связи относятся к дельным, идеализированным типам. В природе не существует с чисто ионными или чисто ковалентными связями. Принято, однако, считать, что в молекулах с одинаковыми атомами связи ковалентны. В молекулах, состоящих из разных атомов, а также в комплексных соединениях химическая связь реализуется сочетанием ионной, ковалентной и других типов связи. [44]
В молекулах атомы элементов связаны между собой ковалентными связями. Молекулы электронейтральны; вещества, состоящие из молекул особенно с чисто ковалентными связями, не проводят электрического тока. [45]
Страницы: 1 2 3 4