Новая ковалентная связь
Cтраница 3
Реакциями нуклеофильного замещения называются такие реакции, когда богатый электронами реагент поставляет свои электроны для образования новой ковалентной связи. Реагенты, несущие отрицательный заряд, а также нейтральные молекулы, имеющие в своем составе атомы со свободными парами электронов, являются нуклеофильными реагентами. [31]
Так как процесс образования связи экзотермичен, рекомбинация дн р к радикалов дает молекулу с полной энергией новой ковалентной связи. Чтобы такая молекула была устойчивой, необходимо отвести избыток энергии за счет колебательного движения или столкновения со стенкой реакционного сосуда или другой молекулой. [32]
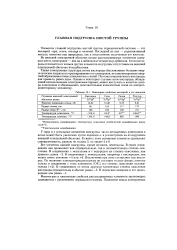 |
Некоторые свойства кислорода и его аналогов. [33] |
Такая электронная структура атома кислорода обусловливает большие энергетические затраты на распаривание его электронов, не компенсируемые энергией образования новых ковалентных связей. Поэтому ковалентность кислорода, как правило, равна двум. Однако в некоторых случаях атом кислорода, обладающий неподеленными электронными парами, может выступать в качестве донора электронов и образовывать дополнительные ковалентные связи по донорно-акцепторному механизму. [34]
Такая пассивность катиона оксония и в этом случае объясняется, вероятно, неспособностью кислорода к расширению октета и образованию новой ковалентной связи или очень высоким окислительно-восстановительным потенциалом катиона оксония. [35]
Они происходят под действием реагентов, несущих отрицательный заряд ( например, при действии иона ОН -), и новая ковалентная связь с атомом углерода возникает за счет пары электронов, предоставляемой реагентом. Реакции нуклеофильного замещения водорода в бензольном ядре встречаются сравнительно редко. [36]
Тем не менее реакция по-прежнему является бимолекулярной, так как молек ла растворителя включена в переходное состояние и происходит образование новой ковалентной связи. [37]
Положительно заряженный атом углерода, присутствующий в ионе карбония, представляет собой чрезвычайно активный центр электро-фильности, обладающий тенденцией к образованию новой ковалентной связи за счет своей свободной орбитали. Для этого требуется взаимодействие с каким-либо нуклеофилом. Активность ионов карбония растет с уменьшением их стабильности. Только очень сильно стабилизированные ионы карбония встречаются в растворе в измеримых концентрациях и то при условии отсутствия достаточно активного нуклеофи-ла. [38]
Поэтому - С1 ( и другие галогены), - NO2 и - SO3H, вступая в бензольное ядро, образуют новую ковалентную связь за счет пары электронов, имеющейся у атома углерода. [39]
Реакциями электрофильного замещения называются такие реакции, при которых бедный электронами атакующий реагент присоединяет к себе пару электронов от атакуемого компонента с образованием новой ковалентной связи. Электрофильными реагентами являются положительно заряженные ионы Н, No и все нейтральные молекулы, в состав которых входят атомы с недоукомплектованными электронными орбиталями. [40]
Швенкер и др. [38] кратко описали процесс термодеструкции тозилатов, мезилатов и других сложных эфиров целлюлозы, заключающийся в отщеплении кислотных групп и образовании новых ковалентных связей. [41]
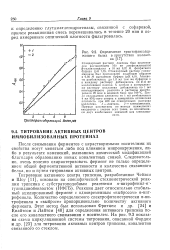 |
Определение триптофансодер-жащего белка в присутствии коллагена. [42] |
После связывания ферментов с нерастворимыми носителями их свойства могут меняться либо под влиянием микроокружения, либо в результате изменений, вызванных химической модификацией благодаря образованию новых ковалентных связей. Следовательно, очень полезно охарактеризовать фермент не только определением общей ферментативной активности и количества связанного белка, но и путем титрования активных центров. [43]
При взаимодействии атомов, имеющих неподеленные электронные пары, с протоном или другим атомом, у которого не хватает до образования октета ( дублета) двух электронов, неподеленная электронная пара становится общей и образует между этими атомами новую ковалентную связь. При этом атом, отдающий электроны, называется донором ( он должен обладать парой неподеленных электронов), а атом, принимающий электроны, называется акцептором. Так, реакция аммиака или аминов с кислотой состоит, по существу, в присоединении протона, отдаваемого кислотой, к неподеленной паре электронов атома азота. [44]
Это объясняется малым размером иона водорода ( протона), который составляет - 10 - 4 от размера атома. Новая ковалентная связь образуется по донорно-акцепторному механизму за счет свободной электронной пары кислорода и является насыщенной. [45]
Страницы: 1 2 3 4