Кратная углерод-углеродная связь
Cтраница 1
Кратная углерод-углеродная связь, сопряженная с электроно-акцепторными группами, такими как - CN, - COOR, - CONH2, - СО -, - N02, - SOOR, вступает в реакции, близкие к альдоль-ной конденсации и имеющие большое практическое значение. [1]
Кратная углерод-углеродная связь, сопряженная с электроно-акцепторными группами, такими как - CN, - COOR, - CONH2, - СО -, - NO2, - SOOR, вступает в реакции, близкие к альдоль-ной конденсации и имеющие большое практическое значение. [2]
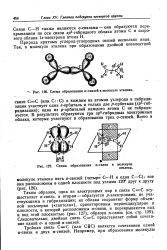 |
Схема образования я-связи в молекуле. [3] |
Природа кратных углерод-углеродных связей несколько иная. [4]
Сопряжение кратных углерод-углеродных связей с группами, проявляющими - С-эффект ( СО, COOR, C N, NO2, SO2 и др.), приводит к увеличению поляризуемости системы, к уменьшению л-электронной плотности кратной углерод-углеродной связи, в результате чего становится возможной нуклеофильная атака на крайний углеродный атом сопряженной системы. [5]
 |
Схема образования ( 7-связей в молекуле этана.| Схема образования а-свя-зей в молекуле этилена. [6] |
Природа кратных углерод-углеродных связей несколько иная. Так, в молекуле этилена при образованиа-д ойной ковалентной связи С С в каждом из атомов углерода в гибридизации участвует одна s - орбиталь и только две р-орбитали ( р2 - гибридизация); одна из р-орбиталей каждого атома С не гибридизуется. В результате образуются три sp2 - гибридных электронных облака, которые участвуют в образовании трех ст-связей. [7]
Названия кратных углерод-углеродных связей и функциональных групп обозначаются суффиксом; суффикс, обозначающий кратную связь ( ен или ин), ставится вместо окончания аи. [8]
 |
Схема образования я-связи в молекуле этилена. [9] |
Природа кратных углерод-углеродных связей несколько иная. [10]
 |
Схема образования о-связей в молекуле этана. [11] |
Природа кратных углерод-углеродных связей несколько иная. Так, в молекуле этилена при образовании двойной ковалентной связи С С ( или С:: С) в каждом из атомов углерода в гибридизации участвует одна s - орбиталь и только две р-орбитали ( sp2 - гибридизация); одна из р-орбиталей каждого атома С не гибри-дизуется. В результате образуются три 5р2 - гибридных электронных облака, которые участвуют в образовании трех а-связей. [12]
 |
Схема образования о-связей в молекуле этана.| Схма образования О-связей в молекуле этилена. [13] |
Природа кратных углерод-углеродных связей несколько иная. Так, в молекуле этилена при образовании двойной ковалентной связи СС ( или С:: С) в каждом из атомов углерода в гибридизации участвует одна s - орбиталь и только две р-орбитали ( sp2 - гибридизация); одна из р-орбиталей каждого атома С не гибри-дизуется. В результате образуются три р2 - гибридных электронных облака, которые участвуют в образовании трех о-связей. [14]
 |
Схема образования о-связей в молекуле этана.| Схеиа образования 0-связей в молекуле этилена. [15] |
Страницы: 1 2 3 4