Взаимодействие - возбужденная молекула
Cтраница 2
Образование Н2, СН4 и других продуктов радиолиза ароматических углеводородов, так же как и в рассмотренных выше случаях, может происходить в процессах первичной диссоциации, в результате вторичных радикальных и ионно-молекулярных реакций и взаимодействия возбужденных молекул. В табл. 37 приведены данные по выходу радикалов при облучении бензола и его производных, а также, для сопоставления, некоторых парафиновых углеводородов. [16]
Образование Н2, СН4 и других продуктов радиолиза ароматических углеводородов, так же как и в рассмотренных выше случаях, может происходить в процессах первичной диссоциации, в результате вторичных радикальных и ионно-молекулярных реакций и взаимодействия возбужденных молекул. В табл. 37 приведены данные то выходу радикалов при облучения бензола и его производных, а также, для сопоставления, некоторых парафиновых углеводородов. [17]
В общем случае эти молекулы могут участвовать в следующих процессах: излучение света возбужденной молекулой ( флуоресценция), потеря энергии при столкновении с какой-либо другой молекулой ( тушение флуоресценции), предиссоциационный распад молекулы и, наконец, взаимодействие возбужденной молекулы с другими молекулами, приводящее к реакции. [18]
В общем случае эти процессы представляют собой: излучение света возбужденной молекулой ( флуоресценция), потерю энергии при столкновении с какой-либо другой молекулой ( тушение флуоресценции), пре-диссоциационпый распад молекулы - спонтанный или индуцированный - если поглощение света приходится на область предиосоциации, и, наконец, взаимодействие возбужденной молекулы с другими молекулами, приводящее к реакции. [19]
В противном случае преобладает окисление синглетным кислородом, даже если кислород присутствует лишь в виде следов. В их отсутствие взаимодействие возбужденной молекулы сенсибилизатора с кислородом приводит лишь к тушению. Реакции фотоокисления с химической сенсибилизацией субстрата преобладают по сравнению с окислением синглетным кислородом, когда высока концентрация субстрата [ R - Н ], а концентрация кислорода [ СЬ ], напротив, мала. Например, они преобладают в насыщенных воздухом растворах, а не в насыщенных кислородом. [20]
Реакции переноса электрона, являясь простейшим типом химического процесса, весьма распространены в фотохимии. Перенос электрона, происходящий при взаимодействии возбужденных молекул с донорами или акцепторами электрона, связан с тем, что при возбуждении молекул уменьшается их потенциал ионизации и возрастает сродство к электрону. Такое взаимодействие возбужденных молекул с донорами и акцепторами электрона приводит к различным химическим и физическим процессам. В малополярных растворителях часто наблюдается образование возбужденных комплексов переноса заряда - эксиплексов. В полярных растворителях, где сольватация понижает энергию эксиплексов, реакция их образования становится необратимой и образуются ион-радикальные пары и свободные ион-радикалы. [21]
Реакции переноса электрона, являясь простейшим типом химического процесса, весьма распространены в фотохимии. Перенос электрона, происходящий при взаимодействии возбужденных молекул с донорами или акцепторами электрона, связан с тем, что при возбуждении молекул уменьшается их потенциал ионизации и возрастает сродство к электрону. Такое взаимодействие возбужденных молекул с донорами и акцепторами электрона приводит к различным химическим и физическим процессам. В малополярных растворителях часто наблюдается образование возбужденных комплексов переноса заряда - эксиплексов. В полярных растворителях, где сольватация понижает энергию эксиплексов, реакция их образования становится необратимой и образуются ион-радикальные пары и свободные ион-радикалы. [22]
Многие молекулы, не взаимодействующие в основных состояниях, при возбуждении образуют довольно стабильные комплексы. Таким образом, эксимер получается при взаимодействии возбужденной молекулы с молекулой той же химической природы, но в основном состоянии, а эксиплекс - при взаимодействии химически различающихся частиц. [23]
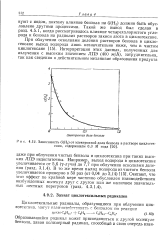 |
Зависимость 0 ( Н2 от электронной доли бензола в растворе циклогексана, содержащем 0 3 М иода. [24] |
Например, выход водорода в циклогексане увеличивается от 5 6 ( у-лучи) до 7 7 при облучении осколками деления ( разд. Считают, что этот эффект по крайней мере частично обусловлен взаимодействием возбужденных молекул друг с другом или же наличием значительных местных перегревов ( разд. [25]
Невыгодно понижать давление поглощающего пара вследствие малости коэффициента поглощения в дискретной области, но можно разбавить пары инертным газом при достаточно большом давлении, чтобы уменьшить взаимодействие возбужденных молекул с нормальными того же сорта. [26]
При наличии связи экситонного типа одиночный уровень изолированной молекулы расщепляется в полосу уровней в кристалле, и, следовательно, низшие экситонные состояния понижены по сравнению с низшими уровнями изолированной молекулы. В результате этого наиболее низкочастотная полоса поглощения молекулярного кристалла испытывает смещение в сторону больших длин волн даже по сравнению с исправленным значением длины волны, учитывающим обычное длинноволновое смещение, обусловленное усиливающимся кулоновым взаимодействием возбужденной молекулы со своими соседями в конденсированной фазе. Исключения появляются в тех случаях, когда переходы на низший экситонный уровень оказываются запрещенными. [27]
Так, величины G ( R) для бензола и циклогексана различаются в 9 - 10 раз, в то время как выходы исходных молекул G ( - / И) различаются всего в 2 раза ( см. стр. Это показывает, что основные процессы превращения ароматических углеводородов происходят не только в результате радикальных реакций, а по-видимому, как и в случае других углеводородов, также в результате ионно-молекулярных реакций и взаимодействия возбужденных молекул. Однако на основании имеющихся данных значение каждого из этих процессов в ра-диолизе ароматических углеводородов пока не может быть определено. [28]
Реакции переноса электрона, являясь простейшим типом химического процесса, весьма распространены в фотохимии. Перенос электрона, происходящий при взаимодействии возбужденных молекул с донорами или акцепторами электрона, связан с тем, что при возбуждении молекул уменьшается их потенциал ионизации и возрастает сродство к электрону. Такое взаимодействие возбужденных молекул с донорами и акцепторами электрона приводит к различным химическим и физическим процессам. В малополярных растворителях часто наблюдается образование возбужденных комплексов переноса заряда - эксиплексов. В полярных растворителях, где сольватация понижает энергию эксиплексов, реакция их образования становится необратимой и образуются ион-радикальные пары и свободные ион-радикалы. [29]
Реакции переноса электрона, являясь простейшим типом химического процесса, весьма распространены в фотохимии. Перенос электрона, происходящий при взаимодействии возбужденных молекул с донорами или акцепторами электрона, связан с тем, что при возбуждении молекул уменьшается их потенциал ионизации и возрастает сродство к электрону. Такое взаимодействие возбужденных молекул с донорами и акцепторами электрона приводит к различным химическим и физическим процессам. В малополярных растворителях часто наблюдается образование возбужденных комплексов переноса заряда - эксиплексов. В полярных растворителях, где сольватация понижает энергию эксиплексов, реакция их образования становится необратимой и образуются ион-радикальные пары и свободные ион-радикалы. [30]
Страницы: 1 2 3