Пространственное взаимодействие
Cтраница 2
На соотношение изомеров влияют также пространственные взаимодействия, например количество жега-изомера в случае 3-за-мещенных аринов возрастает при увеличении объема заместителя или нуклеофила. Атомы водорода в ие / ш-положении также препятствуют подходу объемистых нуклеофилов к 1 2-дегидронафта-лину и 9 10-дегидрофенантрену. [16]
Следует напомнить, что вследствие пространственных взаимодействий зигзагообразная гранс-конформация пинакона ( в которой гидрокспльные группы наиболее далеко разделены) является более стабильной, чем ыс-конформация, из которой может образовываться циклический эфир. Поэтому, как и в случае окисления гликолей йодной кислотой, скорость образования хроматного эфира является важным критерием в определении легкости расщепления гликолей. [17]
 |
Переходные состояния по Фелкину. [18] |
К будет убывать в результате пространственного взаимодействия, которое изображено на рисунке в виде заштрихованной области. [19]
 |
Эмпирические значения параметров в формулах ( 4 - 9 и ( 4 - 10. [20] |
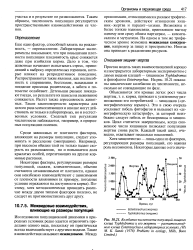
По-видимому, это объясняется эффектами внутримолекулярных пространственных взаимодействий и особенностями тепловых колебаний молекул в кристалле. [21]
Теоретический расчет этой зависимости при пространственном взаимодействии атомов в решетке довольно сложен. Поэтому указанную зависимость находят обычно экспериментально. [22]
Наиболее строгим методом теоретического определения энергии пространственного взаимодействия валентно не связанных атомов в активированном комплексе является такой расчет, который основывался бы на данных о ван-дер-ваальсовых кривых отталкивания атомов, сближающихся на расстояние, меньшее суммы соответствующих межмолекулярных радиусов. Такое взаимодействие может приводить к искажению валентных углов и растяжению связей в исходных молекулах. Поэтому для точного расчета необходимы также силовые константы деформации валентных углов и растяжения соответствующих связей. Если располагать всеми этими данными, то можно найти минимальное значение суммы рассмотренных энергий взаимодействия; тем самым одновременно была бы решена также задача определения конфигурации активированного комплекса. [23]
Обе кон-формации равноценны также и по пространственному взаимодействию групп R и R, а поэтому и равновероятны. [24]
Таким образом, численность популяции регулируется пространственными взаимодействиями ее членов. [26]
По мере роста объема радикала усиливаются его неблагоприятные пространственные взаимодействия с карбонильным кислородом, и доля Z-формы падает. Барьер вращения AG для грет-бутилацетамида составляет 80 кДж / моль, при переходе к триметилсилильному аналогу он понижается до 68 кДж / моль, что объясняют р - d - электронным взаимодействием. [27]
По мере роста объема радикала усиливаются его неблагоприятные пространственные взаимодействия с карбонильным кислородом, и доля Z-формы падает. Барьер вращения AG для грег-бутилацетамида составляет 80 кДж / моль, при переходе к триметилсилильному аналогу он понижается до 68 кДж / моль, что объясняют р - - электронным взаимодействием. [28]
Бензольные кольца выталкиваются из копланарной конфор-мации вследствие пространственного взаимодействия о - Н - ато-мов соседних ядер друг с другом. Как и следовало ожидать, было найдено, что о-заместители, более объемистые, чем атом водорода, увеличивают диэдральный угол ( поворот кольца по отношению к положению в копланарной конформации) ароматического кольца до 50 и более. Это, конечно, должно быть обусловлено стерическим эффектом: о-заместители очень близко расположены к радикальному атому углерода и поэтому мешают его приближению к другой частице или мешают другим частицам приближаться к нему [ ср. [29]
Такие миграции обычно протекают в направлении уменьшения пространственных взаимодействий между заместителями. [30]
Страницы: 1 2 3 4