Ион-дипольное взаимодействие
Cтраница 2
Ионы за счет ион-дипольного взаимодействия способны притягивать полярные молекулы других веществ. Поэтому ионные кристаллы хорошо растворимы в полярных жидкостях, молекулы которых вытягивают из кристалла ионы и, окружая их, нарушают ионные связи. Подробнее механизм растворения рассматривается в гл. [16]
У Расчет энергии ион-дипольного взаимодействия ионов с молекулами, находящимися во вторичной гидратной ( сольват-ной) оболочке, показывает, что эта энергия на порядок меньше средней энергии теплового движения. [17]
Отсюда следует, что ион-дипольные взаимодействия облегчают диссоциацию ионных пар. Поэтому, чем выше дипольный момент молекул среды или чем больше их число, приходящееся на единицу объема, тем сильнее ион-дипольные взаимодействия между ионами и дипольными молекулами растворителя. [18]
Таким образом, теория адсорбционного ион-дипольного взаимодействия в первом приближении подтверждается экспериментально. [19]
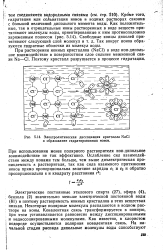 |
Электролитическая диссоциация кристалла NaCl и образование гидратированных ионов. [20] |
При использовании менее полярного растворителя ион-дипольное взаимодействие не так эффективно. [21]
В кислородных стеклах в результате ион-дипольного взаимодействия между этими соединениями и окислами-стеклообразователями может образоваться непрерывная пространственная структура. [22]
Если для данной системы энергия ион-дипольного взаимодействия больше энергии диполь-дипольного, молекула растворителя считается прочно связанной с ионом. Выражение для энергии диполь-дипольного взаимодействия между молекулами воды, находящимися вблизи иона, и молекулами воды в массе раствора содержит величину, представляющую собой координационное число иона по отношению к воде. Кривая потенциальной энергии координации молекул воды, окружающих ион, проходит через максимум при определенном значении п, характерном для каждого иона. [23]
Если ион, участвующий в ион-дипольном взаимодействии, замещают на другую полярную молекулу, то создается ситуация для возникновения диполъ-диполъного взаимодействия. Отметьте, что молекулы воды на рис. 2 - 5, а расположены таким образом, что противоположно заряженные концы полярных молекул сближены. [24]
 |
Ориентационное ( а, индукционное ( б и дисперсионное ( в взаимодействие молекул ( М - неполярная молекула. [25] |
К межмолекулярному взаимодействию относятся также и ион-дипольное взаимодействие. [26]
 |
Схема взаимодействия со - J. [27] |
К ним относятся водородная связь и ион-дипольное взаимодействие. [28]
Энергия специфической сольватации катиона дополняется энергией неспецифического ион-дипольного взаимодействия катионов и анионов с полярными молекулами растворителя. [29]
Что касается членов, характеризующих изменение ион-дипольного взаимодействия свободных и ассоциированных ионов в воде и неводном растворителе, то нет оснований считать, что эти изменения для обоих ионов будут сильно отличаться друг от друга. [30]
Страницы: 1 2 3 4