Хлорный ангидрид
Cтраница 4
Водоотнимаю-щие средства применяются в количестве, несколько меньшем эквивалентного количеству связываемой воды, с расчетом, чтобы часть хлорной кислоты осталась в виде моногидрата для предотвращения образования хлорного ангидрида. Расход водоотнимающих соединений определяется эмпирически, с учетом выхода хлорной кислоты и ее концентрации. В лабораторных условиях отгонка ведется из колбы типа Кляйзена. [46]
Для того чтобы связать и идеи - пературы при растворении тифицировать промежуточные про - чистого хлорного ангидрида дукты, авторы провели разложение ( - 0 и смеси С12О7 и НСЮ4 ( 2) хлорного ангидрида в присутствии различных количеств фтора. В присутствии достаточных количеств фтора скорость распада С12О7 заметно сокращается, общее время реакции ( до прекращения изменений давления в системе) уменьшается и соответствует примерно 1 5 периода полураспада незатрудненной реакции, давление газов к концу процесса иногда бывает меньше исходного. В присутствии фтора лишь несколько процентов С12О7 распадается на хлор и кислород, большая часть ангидрида ( - 95 %) переходит в хлорил - и перхлорилфторид. [47]
При потенциалах выше 2 6 - 2 7 В на аноде протекают процессы с участием хемосорбировапных радикалов и образуются новые продукты высокой степени окисления: при электролизе серной кислоты - надсерная кислота; при электролизе хлорной кислоты - хлорный ангидрид; при электролизе растворов карбоповых кислот и их солей - этана, диметилсебацината и др. Низкая температура оказывает стабилизирующее действие на адсорбированные лабильные промежуточные частицы и способствует повышению выхода по току перечисленных выше продуктов. [48]
В работе [8] было показано, что, если очень медленно приливать безводную хлорную кислоту к охлажденному до - 78 С фосфорному ангидриду и затем отгонять С12О7 в вакууме, не поднимая температуру реакционной смеси выше - 30 С, то бесцветный хлорный ангидрид удается получить без дополнительной перегонки. Еще лучшие результаты дает взаимодействие фосфорного ангидрида с парами хлорной кислоты при - 30 С и использовании вместо Р205 серного ангидрида, растворенного в серной кислоте. В последнем случае удается полностью избежать образования низших окислов хлора. [49]
Как показано в разделе 3 и 4, разряжающиеся частицы HSO - и ClOj благодаря наличию окислов на платиновых электродах слабо связываются с поверхностью платины, сохраняют свойства радикалов и проявляют способность к димеризации с образованием перекисных соединений, что приводит к реакции синтеза соответственно надсерной кислоты и хлорного ангидрида. Больше того, ряд соединений, например углеводороды, диссоциирующие на водород и углеродсодержащий остаток, при адсорбции на металлических электродах типа платины, благодаря низкой энергии адсорбции водорода на окисленной поверхности остаются недиссоциированными и сохраняют способность присоединять кислород, давая продукты синтеза. [50]
 |
Состав пара над растворами. [51] |
Чистый хлорный ангидрид - бесцветная жидкость с температурой плавления - 90 2 С; при получении, а также при хранении он может окрашиваться низшими оксидами хлора. Хлорный ангидрид имеет сравнительно низкую химическую активность. При комнатной температуре он не реагирует с серой, фосфором и бромом, растворяется без взаимодействия в ССЦ; при попадании капли ангидрида на дерево или бумагу он испаряется без взрыва. [52]
С) отвечает формуле ОзС1 - О-СЮз. Хлорный ангидрид смешивается с четыреххлористым углеродом в любых соотношениях. Энергия этой связи оценивается в 48 ккал / моль. [53]
С) отвечает формуле О С1 - О-СЮз. Хлорный ангидрид смешивается с четыреххлористым углеродом в любых соотношениях. Энергия этой связи оценивается в 48 ккал / моль. [54]
В течение периода индукции происходит накопление окислов хлора в жидкой фазе. Уменьшение концентрации хлорного ангидрида пополняется сдвигом равновесия вправо. Скорость расходования С1207 значительно меньше скорости его поступления, так что стационарная концентрация ангидрида в процессе распада, вероятно, близка его равновесной концентрации. [55]
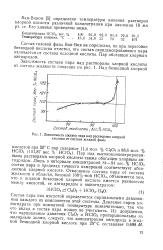 |
Зависимость состава пара над растворами хлорной кислоты от состава жидкой фазы. [56] |
Состав газовой фазы Ван-Вик не определял, но при перегонке безводной кислоты отметил, что состав сконденсированного пара отличается от состава исходной кислоты. Пар обогащен хлорным ангидридом. [57]
Страницы: 1 2 3 4