Диоксидифенилметана
Cтраница 1
Диоксидифенилметаны взаимодействуют с формальдегидом или фенолоспиртами. Дальнейшее последовательное присоединение и конденсация приводят к росту линейной цепи, в которой фенольные ядра связаны метиленовыми мостиками. Скорость конденсации намного выше, чем присоединение, вследствие чего в молекулах олигомеров содержится небольшое число мети-лольных групп. [1]
Сульфирование и - диоксидифенилметана было проведено путем нагревания указанного соединения с пятикратным по весу количеством сульфирующей смеси ( 2 / 3 концентрированной серной кислоты 1 / 3 олеума, содержащего 30 % свободного S03) при нагревании на водяной бане в продолжении одних суток. [2]
Титрование и - диоксидифенилметана описано в гл. [3]
Алкилированные в ядро производные диоксидифенилметана можно получать нагреванием 2 4-диалкилфенола с формальдегидом в присутствии сильной кислоты. [4]
Положение о том, что диоксидифенилметаны являются промежуточными продуктами, было подтверждено многими исследователями. Так, Мегсон и Друммонд [4] показали, что количество диоксидифенилметанов, которое может быть выделено из феноло-формальдегидной реакционной смеси, в начале реакции повышается, а затем падает; следовательно, они являются промежуточными продуктами реакции, которые затем превращаются в смолы. [5]
Например, сплавленные в различных соотношениях диоксидифенилметаны неограниченно долго сохраняли смолообразное состояние. Известно также, что добавка 8 % пирокатехина к бензофенону, который в чистом виде способен счень быстро кристаллизоваться, уменьшает скорость кристаллизации в 4 раза. В качестве примера можно привести также канифоль, которая встречается в природе в нескольких видах. Испанская канифоль, в состав которой входит пимаровая кислота, в отличие от американской, состоящей в основном из абиетиновой кислоты, нестабильна в смолообразном состоянии и через некоторый промежуток времени приобретает кристаллическую структуру. [6]
В присутствии щелочных катализаторов процесс идет иначе: диоксидифенилметаны не образуются, а получаются неустойчивые при нагревании фенолоспирты, превращающиеся в растворимые смолы; последние при дальнейшем нагревании образуют резиноиды. [7]
Смолы на основе / г / г - диоксидифенилметана характеризуются более высокой теплостойкостью в отвержден-ном состоянии по сравнению со смолами из дифенилол-пропана. [8]
Аналогичным образом получаются и четырехъядерные и высшие производные диоксидифенилметана. [9]
Аналогичным образом получаются и четырехъядерные и высшие производные диоксидифенилметана. [10]
Брауном & ь установлено, что причиной малой термостабильности производных диоксидифенилметана является наличие свободной гидроксильной группы. Сложные и простые бис-эфиры значительно устойчивее. Поэтому при получении ароматических поликарбонатов методом переэтерификации рекомендуется брать небольшой избыток дифенилкарбоната, а также предотвращать удаление последнего при отгонке фенола. [11]
В продуктах щелочной конденсации фенола находится много о, я - диоксидифенилметана, а продукты кислой конденсации в основном содержат п п - производные. [12]
Соответственно этому Ламберт75 с целью получения антиокси-дантов для каучука среди других синтезировал следующие несимметрично замещенные диоксидифенилметаны. [13]
Соответственно этому Ламберт75 с целью получения антнокси дантов для каучука среди других синтезировал следующие несимметрично замещенные диоксидифенилметаны. [14]
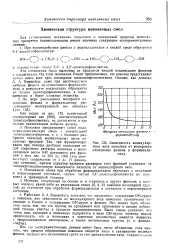 |
Зависимость молекулярного веса новолака от молярного отношения фенола к формальдегиду. [15] |
Страницы: 1 2 3