Диоксидифенилметана
Cтраница 3
При конденсации в кислой среде при соотношении фенола и формальдегида 7: 6 через 20 - 30 мин. Для двух полученных таким образом смол характерно отличие в среднем молекулярном весе и содержании свободного фенола. Если эти смолы осаждением из спирта водой или перегонкой в глубоком вакууме очистить от свободного фенола и диоксидифенилметана, то они будут представлять собой твердые продукты, которые при дополнительной обработке формальдегидом способны переходить в ре-зольные смолы и отверждаться в резиты. [31]
Эти соединения были выделены из продуктов кислой конденсации фенолов с альдегидами. На этом основании Рашиг предположил, что новолак представляет собою смесь всех трех изомерных диоксидифенилметанов. Однако, как доказал - Ваншейдт, даже при десятикратном избытке фенола по отношению к формальдегиду в результате конденсации образуются но только диоксидифенилметаны, а одновременно и более сложные вещества. [32]
Для уточнения условий синтеза исследовали конденсацию индивидуальных алкилфенолов ( п-трет-бутл -, п-трет-аынл - и ге-гуэег-октилфенола) с формальдегидом. В результате были получены 5 5 -диалкил - 2 2 -диоксидифенил-метаны, физические константы которых соответствовали теоретически вычисленным. Затем 5 5 -диалкил - 2 2 диоксидифенилметаны обрабатывали гидроокисью, бария. [33]
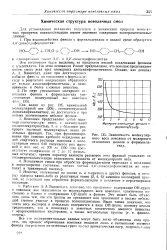 |
Зависимость молекулярного веса новолака от молярного отношения фенола к формальдегиду. [34] |
Эти соединения были выделены из продуктов кислой конденсации фенолов с альдегидами. На этом основании Рашиг предположил, что новолак представляет собою смесь всех трех изомерных диоксидифенилметанов. Ваншейдт, даже при десятикратном избытке фенола по отношению к формальдегиду в результате конденсации образуются н только диоксидифенилметаны, а одновременно и более сложные вещества. [35]
Фенол ( СеНвОН) не реагирует с формальдегидом в нейтральных водных растворах ни на холоду, ни при нагревании. Реакция между ними начинается и протекает только с помощью катализаторов - гидроксильных или водородных ионов. Нужная для реакции концентрация водородных ионов достигается введением в реакционную смесь кислот, щелочей или веществ, гидролитически расщепляющихся с образованием водородных или гидроксильных ионов. Многоатомные и различные замещенные фенолы могут реагировать с формальдегидом в нейтральном водном растворе, если они имеют более выраженные, чем у простейшего фенола, кислые свойства. Точно так же простейший фенол может вступать во взаимодействие с альдегидами в нейтральном растворе, если эти альдегиды имеют кислые свойства вследствие наличия у них кислых замещающих групп. При высоких концентрациях водородных ионов среди начальных продуктов конденсации фенола с формальдегидом преобладают изомерные диоксидифенилметаны. Высокие концентрации гидроксильных ионов благоприятствуют присоединению больших молярных количеств формальдегида к фенолу и приводят к преобладанию изомерных оксибензиловых спиртов и вообще продуктов с конечными метилольными группами. Наличие последних является одним из факторов, предотвращающих выпадение из растворов продуктов щелочной конденсации даже сравнительно большого молекулярного веса. Продукты кислой конденсации выпадают из раствора уже в самом начдде реакции и имеют сравнительно небольшой молекулярный вес. Малая растворимость ( выпадение из сферы реакции) начальных продуктов фенол альдегидной конденсации в кислой среде и отсутствие в них достаточного количества метилольных групп являются факторами, неблагоприятными для получения резольных смол. При работе с маслорастворимыми фенолами или альдегидами в реакционную смесь вводят в качестве дополнительных катализаторов смачивающие вещества, создающие реактивный контакт между молекулами фенолов и альдегидов. [36]
Страницы: 1 2 3