Диполь - связь
Cтраница 1
Диполи связей С-О и О - Н направлены в сторону атома кислорода. [1]
Что представляет собой диполь связи. [2]
Соответственно в четных алканах диполи концевых связей противонаправлены и компенсируют друг друга. Можно было бы предположить, что молекулы нечетных алканов полярны, а молекулы четных алканов неполярны. Однако это может быть справедливо только для твердых алканов, так как в твердой фазе большая часть молекул находится в полностью трансоидном конформашюнном состоянии. В жидкости же преобладают скошенные конформации. [3]
Соответственно в четных елканах диполи концевых связей противонаправлены и компенсируют друг друга. Можно было бы предположить, что молекулы нечетных алканов полярны, а молекулы четных алканов неполярны. Однако это может быть справедливо только для твердых алканов, так как в твердой фазе большая часть молекул находится в полностью трансоидном конформационном состоянии. В жидкости же преобладают скошенные конформации. [4]
Эффекты, первопричиной которых являются диполи связей, называются индуктивными эффектами, они в значительной мере определяют многие химические и физические свойства органических молекул. Однако во многих случаях заместители могут взаимодействйвать с остальной частью молекулы также и по другим механизмам; Детальное понимание эффектов заместителей зависит: от возможности разделения этих различных факторов. Эта проблема будет обсуждаться более обстоятельно в гл. [5]
Поскольку молекула CS2 линейная, диполи связей С-S компенсируют друг друга, и результирующий дипольный момент молекулы равен нулю. Молекула H2S изогнутая, поэтому диполи связей Н - S не компенсируют друг друга. Молекула имеет результирующий дипольный момент. [6]
В случае СН3СНСНС1, поскольку диполи связей СНз-С и С1 - С имеют противоположное направление, транс-изомер имеет больший дипольный момент и более высокую температуру кипения. Устойчивость не обязательно коррелируется с дипольным моментом: для бутена-2 более устойчивым является граяс-изомер, а для двух остальных соединений - цис-нзомер. Причины такого порядка устойчивости не вполне понятны; по-видимому, пространственное отталкивание преобладает в случае бутена-2, в то время как для более поляризуемых галогенных соединений силы притяжения Лондона доминируют в случае ыс-изомеров. [7]
Неравномерное распределение электронной плотности в ковалентной связи создает диполь связи, в качестве единицы измерения4 которого служит произведение заряда на расстояние ( для более детального обсуждения ем. [8]
Поскольку X и Y всегда сильно электроотрицательны, диполи связей X - Н и Y - Н должны быть значительными. Далее, ввиду того что атом водорода, не имеющий внутренних электронных оболочек, очень мал, возможно значительное сближение этих диполей. Это не исключает наличия резонансного вклада в прочность водородной связи. Для симметричных водородных связей, по крайней мере некоторых, такой вклад может быть столь же существенным, как и электростатический. [9]
Следует отметить, что эффективный поверхностный диполь л и диполь связи адсорбат - атом металла не обязательно находятся в простом соотношении. В некоторых случаях, например при адсорбции водорода на ряде металлов, эти величины имеют даже разные знаки. Относительно множителя 4я в уравнении ( 39) см. гл. [10]
Разность электроотрицательностей атомов Н и О довольно значительна, поэтому диполи связей Н8 - О5 - велики; электроотрицательно-сти атомов О и F отличаются не так сильно, поэтому диполи связей F8 - О8 малы. [11]
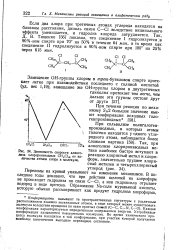 |
Зависимость скорости алкого-лиза хлорпроизводных СН С1т от количества атомов хлора в молекуле. [12] |
Если два хлора при третичных атомах углерода находятся на близком расстоянии, диполь связи С - С1 вследствие вицинального эффекта уменьшается, и гидролиз хлорида затрудняется. Так, Д. В. Тшценко [56] показал, что соединение I гидролизуется в 90 % - ном спирте при 70 на 50 % в течение 64 мин, в то время как соединение II гидролизуется в 90 % - ном спирте при 100 на 25 % через 615 мин. [13]
Если два хлора при третичных атомах углерода находятся на близком расстоянии, диполь связи С - С1 вследствие вицинального эффекта уменьшается, и гидролиз хлорида затрудняется. Так, Д. В. Тищенко [48] показал, что соединение I гидролизуется в 90 % - ном спирте при 70 на 50 % в течение 64 минут, в то время как соединение II гидролизуется в 90 % - ном спирте при 100 на 25 % через 615 минут. [14]
Так, из ныоменовской проекции молекулы р-аномера вдоль связи С-1-О-5 можно видеть, что диполь связи С-1-X параллелен диполю кислородного атома цикла, вследствие чего отталкивание между этими диполями сильнее, чем в случае а-аномера. [15]
Страницы: 1 2 3