Дипропиламин
Cтраница 3
Чувствительность в определяемом объеме: для пирролидина - 2 мкг; пиперидина - 3 мкг; гексамети-ленимина, морфолина, диаллиламина, диизопропилами-на, дипропиламина - 5 мкг; для моноизопропиламина и моноаллиламина - - 10 мкг. [31]
Бензины: А-66, А-72, А-76, Б-70 Галоша, экстракционный по ГОСТ 462 - 51, экстракционный по МРТУ 12Н - 20 - 63; бутил хлористый, бутилметакрилат, винилциклогексен, гексан, гептан, диизобутиламин, диметиламиноэтанол, N, N-диметилпропандиамин - 1 3 дипропиламин, диэтиламиноэтанол, изовалериано-вый альгедид, изооктилен, ингибиторы коррозии металлов: И-21-Д, И-ЗО-Д; камфен, керосин, лаки: ПЭ-250, ПЭ-232; метиловый эфир, Р - метоксипропио-новой кислоты, морфолин, нефть, пентан, петролей-ный эфир, полиэфир ТГМ-3, растворитель № 651, сероокись углерода, скипидар, спирт амиловый, те-трагидроинден, тетрафторэтилен, топливо: Т-1, TC - lf Т-6, Т-8, печное марки А; триметиламин, уайт-спи. [32]
Этот метод позволяет, используя в недостатке аммиак или амин, получить в обоих случаях только один продукт. Получение дипропиламина по методу Гофмана в одну стадию привело бы неизбежно к смеси ди - и трипропиламипов. [33]
Технологический процесс получения эптама состоит из двух основных стадий: получение дипропилкарбамоилхлорида и получение эптама. Синтез исходного дипропиламина осуществляется при взаимодействии нормального пропилового спирта и аммиака на катализаторе при температуре 200 С и давлении водорода 30 ат. [34]
Второй стадией реакции озонирования эптама является окисление этилмеркаптана, сопровождающееся образованием сульфокислот и понижением рН раствора. На третьей стадии окисляется дипропиламин и остаточные количества эптама. Отмечено, что одним из основных факторов, влияющих на процесс озонирования амина, является значение рН среды. Расход озона, обеспечивающий 100 % - е разложение дипропиламина в обрабатываемой воде при рН 8 5, составляет 8 моль на 1 моль или 3 8 мг на 1 мг вещества. На рис. 13 приведены данные, характеризующие окисление дипропиламина озоном и поглощение озона в этой реакции. Время разложения амина определяется скоростью поступления озона в реактор. В продуктах реакции идентифицированы карбоновые кислоты и натрат-ионы. [35]
Растворимость в воде при 20 С 90 мг / л, смешивается во всех отношениях с ксилолом, метилэтилкетоном, метилизобутилкетоном и циклогексано-ном. В щелочной среде гидролизуется с образованием дипропиламина, про-пантиола и карбоната щелочного металла. [36]
Растворимость в воде при 20 С 90 мг / л, смешивается во всех отношениях с ксилолом, метилэтилкетоном, метилизобутилкетоном и циклогексаноном. В щелочной среде гидролизуется с образованием дипропиламина, пропилмеркаптана и карбоната щелочного металла. [37]
В щелочной среде гидролизуется с образованием дипропиламина, пропил-меркаптана и карбоната щелочного металла. Разрушается микроорганизмами почвы за 1 5 - 2 месяцев. [38]
Растворимость в воде при 20 С 90 мг / л, смешивается во всех отношениях с ксилолом, метилэтилкетоном, метилизобутилкетоном и циклогексаноном. В щелочной среде гидролизуется с образованием дипропиламина, пропилмеркаптана и карбоната щелочного металла. [39]
Так, диэтил-амин кипит при 56 С, а бутиламин - при 76 С, н-гексиламин ( первичный) кипит при 129 С, дипропиламин ( вторичный) - при 110 7 С, а триэтиламин ( третичный) - при 89 5 С. [40]
Так, диэтиламин кипит при 56 С, а бутиламин - при 76 С, н-гексиламин ( первичный) кипит при 129 С, дипропиламин ( вторичный) - при 110 79С, а три-этиламин ( третичный) - при 89 5 С. [41]
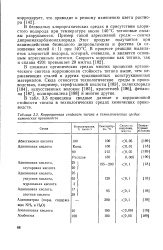 |
Коррозионная стойкость титана в технологических средах химических производств. [42] |
В безводных хлорорганических средах в присутствии хлористого водорода при температуре около 140 С титановые сплавы разрушаются. Этот продукт получается при взаимодействии безводного дипропиламина и фосгена ( в отношении молей 4: 1) при 140 С. В процессе реакции выделяется хлористый водород, который, очевидно, и является основным агрессивным агентом. [43]
В безводных хлорорганических средах в присутствии хлористого водорода при температуре около 140 С титановые сплавы разрушаются. Примером такой агрессивной среды является синтез дипропилкарбамоилхлорида. Этот продукт получается при взаимодействии безводного дипропиламина и фосгена ( в отношении молей 4: 1) при 140 С. В процессе реакции выделяется хлористый водород, который, очевидно, и является основным агрессивным агентом. [44]
Добавляют 5 мл анализируемого раствора к смеси 20 мл буферного раствора, 5 мл 1 % - ного раствора нитропруссида натрия в 10 % - ной уксусной кислоте и 5 мл 10 % - ного раствора уксусного альдегида. Оптическую плотность фиолетово-синего раствора измеряют через 20 мин при 560 - 600 нм. Таким способом определяют диметиламин, диэтил-амин, дипропиламин и другие вторичные амины. [45]
Страницы: 1 2 3 4