Сравнение - скорость - реакция
Cтраница 2
Значение Н2О как мостиковой группы можно наглядно проиллюстрировать сравнением скоростей реакций Сг24 с [ Со ( МН3) б ] 3 и с [ Со ( NH3) 5H2O ] 3; в первом случае скорость реакции по крайней мере в 100 раз меньше. Это объясняют отсутствием в координированной молекуле МНз свободной электронной пары и наличием такой пары в координированной молекуле Н2О, благодаря чему и возможно образование мостика. [16]
Определяя показатели кинетического уравнения, целесообразно при изменении каждого параметра производить сравнение скорости реакции при нескольких степенях превращения. [17]
Авторам известны единственные данные Горинга и др. [71], которые позволяют провести сравнение скоростей реакции углерода с водородом со скоростями вышеназванных реакций углерода с газами. В этой работе приведены данные по реакционной способности древесного угля с водородом и со смесями водорода с парами воды при 870 и общем давлении 1 - 6 атм при 10 % - ном выгорании углерода. Экстраполяция данных на 0 1 атм и 870 дает скорости 5 5 - 10 - 5 и 1 3 - Ю 8, выраженные в граммах газифицированного углерода на грамм углерода в реакторе в секунду для паров воды и водорода соответственно. [18]
Замедление обменной реакции, катализируемой кислотой при положительном заряде субстрата, подтверждено экспериментально сравнением скоростей реакций обмена водорода в ароматических углеводородах. [19]
Замедление обменной реакции, катализируемой кислотой при положительном заряде субстрата было подтверждено экспериментально путем сравнения скоростей реакций обмена водорода в ароматических углеводородах. [20]
Например, при взаимодействии красителя формулы ( 1) с водой при 60 С и рН 10 сравнение скоростей реакции для Х С1 и для X F показывает, что в случае фтора реакция протекает приблизительно в 170 раз быстрее. [21]
Необходимо также иметь в виду, что если пористость сравниваемых катализаторов различна, это может повлечь разную степень внутренне-диффузионного торможения и сравнение скоростей реакций тогда потеряет смысл. [22]
После поправки на гидролиз и на 30-кратное уменьшение реакционной способности эфира с более длинной цепью по сравнению с ацетатом ( что следует из сравнения скоростей реакций с этиламином и, по-видимому, вызвано стерическими препятствиями) найдено увеличение скорости приблизительно в 100 раз в реакции дециламина с эфиром декановой кислоты по сравнению с ацетатом. [23]
Как считает Гальперн, возможность количественного рассмотрения этих процессов представляется очень редко, однако можно определить влияние некоторых факторов на скорость переноса, а качественное обсуждение таких зависимостей в отдельных случаях часто оказывается полезным, особенно при сравнении скоростей реакций или предсказании неизвестных скоростей на основании уже известных. Одно важное ограничение, налагаемое на процессы переноса, состоит в том, что спин электрона не может легко изменяться при переносе и любое предполагаемое превращение, требующее изменения спина электрона, очевидно, протекает медленно. Такое изменение, вероятно, должно происходить через возбужденное состояние одного реагирующего вещества. [24]
Для каждого спирта получалась другая скорость этерификации, тем не менее по величине этой скорости оказалось возможным отличить спирты первичные, вторичные и третичные друг от друга, так как скорости этерификации внутри каждой группы изменяются в довольно узких пределах, тогда как при сравнении скоростей реакций трех групп спиртов наблюдается очень большая разница. [25]
Обрыв цепей происходит на стенках сосуда и в его объеме. Сравнение скоростей реакций 1 и 2 показывает, что в условиях опытов отношение скоростей этих реакций менялось в интервале 10 - 103, что позволяет считать реакцию 1 основной, определяющей особенности процесса. Поэтому факторы, определяющие концентрацию атомарного кислорода в ходе процесса, должны определять и все особенности наблюдаемых на опыте закономерностей. [26]
Самым простым методом оценки активности различных металлов в одной и той же реакции служит сравнение температуры или температурных интервалов, необходимых для получения одинаковых скоростей реакции на каждом металле. Сравнение скоростей реакции при одной определенной температуре менее удобно, поскольку это часто связано со значительной экстраполяцией экспериментальных данных и с необоснованным допущением о постоянстве энергии активации в широком интервале температур. Нельзя получить исчерпывающей характеристики каталитической активности, охватывающей изменение как энергии активации, так и частотного фактора на различных катализаторах до тех пор, пока не будет получено значительно больше сведений об относительной прочности адсорбционных связей реагентов и различных образующихся из них соединений. [27]
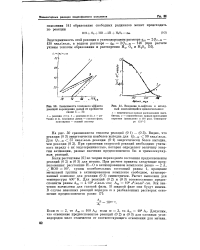 |
Зависимость теплового эффекта реакций зарождения цепей от прочности связи С - Н.| Введение а-нафтола в исходный окисляющийся циклогексанол. [28] |
Видно, что реакция ( О 3) энергетически наиболее выгодна для Qc - н С 90 ккал / моль. При сравнении скоростей реакций необходимо учитывать наряду с их эндотермичностью, которая определяет величину энергии активации, разные значения предэкспонентов би - и тримолекуляр-ных реакций. [29]
Таким образом, влияние электронных факторов на скорость реакций в присутствии металлических катализаторов может быть различным, и в каждом отдельном случае следует учитывать механизм процесса, природу лимитирующей стадии и возможность их изменений при переходе от одного катализатора к другому. Разумеется, сравнение скорости реакции в ряду металлов с разными электродными свойствами возможно только при сохранении неизменными механизма и кинетики / процесса. Без уверенности в этом сопоставление величин скорости реак - ч; ции на разных катализаторах вообще теряет смысл. [30]
Страницы: 1 2 3 4