Среда - инкубация
Cтраница 2
Активация миозиновой АТФазы может быть также достигнута путем внесения в среду инкубации неполярных или слабополярных органических растворителей, что свидетельствует о важной роли гидрофобных взаимодействий в осуществлении регуляции активности миозина. [16]
Измерение скорости потребления кислорода можно проводить манометрически в той же среде инкубации. [17]
В четыре конические колбочки на 25 мл наливают по 3 мл среды инкубации одного из следующих составов: 1) 0 3 М сахароза; 2) 0 25 М сахароза, 3 мМ фосфат калия ( рН 7 4), 15 мМ MgCb, 10 мМ трис - НС1 буфер ( рН 7 4), 5 мМ сукцинат калия; 3) то же, что ( 2), но без фосфата; 4) то же, что ( 2), плюс 100 мкМ 2 4-динитрофенол. [18]
Проводят спетрофотометрические измерения концентрации примесного ( загрязнение реактивов) Са2 в среде инкубации с подходящим металлохромным индикатором. Анализируют причины отклонения от линейности зависимости скорости исследуемого процесса от концентрации белка митохондрий. [19]
Известно, что степень неспецифического восстановления тетразо-лиевых солей возрастает с увеличением рН среды инкубации, а при рН 9 - 10 образование окрашенных продуктов может идти самопроизвольно. [20]
Так как в процессе активного транспорта катионов происходят активация дыхания и закисление среды инкубации, для выполнения работы может быть использована как полярографическая, так и рН - метрическая техника. Из-за трудностей, которые могут возникнуть при изменении скорости дыхания в присутствии низких концентраций катионов, предпочтение следует отдать рН - метрической технике для регистрации кинетики транспортного процесса. [21]
Интактные митохондрии представляют собой осмотически активные пузырьки, отделенные от гиалоплазмы ( или среды инкубации при эксперименте in vitro) двумя мембранами. Таким образом, существуют четыре топологически различных пространства: внешняя мембрана, межмембранное пространство, внутренняя мембрана и внутреннее пространство - матрикс. Ферменты цикла трикарбоновых кислот сосредоточены в матриксе; компоненты дыхательной цепи, транслоказа адениннуклеотидов и АТФ-синтетазный комплекс прочно связаны с внутренней мембраной, в межмембранном пространстве локализована аденилаткиназа, а во внешней мембране - моноаминооксидаза. [22]
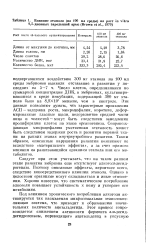 |
Влияние этанола ( на 100 мл среды на рост in vitro 9 5-дневных зародышей крыс ( Brown et al., 1979. [23] |
Число клеток, определявшееся по суммарной концентрации ДНК, в эмбрионах, культивировавшихся в среде инкубации, содержащей 300 мг этанола было на 8 9Х105 меньше, чем в контроле. Эти данные позволяют думать, что характерные проявления АСП - задержка роста, микроцефалия, короткие, деформированные глазные щели, недоразвитие средней части лица и челюстей - могут быть следствием замедления пролиферации клеток па этапе органогенеза. Сопровождающая микроцефалию умственная отсталость может быть следствием задержки роста и развития нервной ткани на ранних этапах внутриутробного развития. Таким образом, описанные нарушения развития возникают не вследствие материнского эффекта, а за счет прямого влияния на развивающийся организм этанола или его метаболитов. [24]
Значительные количества Са2 могут быть накоплены в митохондриях только в присутствии проникающего аниона в среде инкубации, например фосфата или ацетата. Перенос фосфата через мембрану осуществляется с помощью специфического фермента-переносчика, активность которого подавляется низкими концентрациями SH-ядов. Добавление АДФ или Са2 в таких условиях не стимулирует дыхания. Последующее добавление ацетата, перенос которого нечувствителен к этим ядам, стимулирует дыхание и обеспечивает транспорт добавленного ранее Са2 во внутреннее пространство митохондрий. [25]
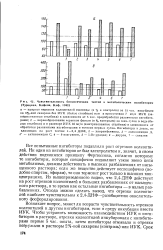 |
Чувствительность биологических тестов ( Турецкая, Кефели, Коф, 1968. [26] |
Возникает вопрос, может ли возрасти чувствительность отрезков колеоптилей к другим ингибиторам, если в среду инкубации ввести ИУК. Чтобы устранить возможность взаимодействия ИУК и ингибиторов в растворе, отрезки колеоптилей инкубировали с ингибиторами первые 5 час. [27]
Так как рН буферных растворов изменяется с изменением температуры, особое внимание обращается на контроль рН используемой среды инкубации. Определение активности Са-АТФазы целесообразно проводить во всем диапазоне температур одновременно. [28]
Результаты опытов по выявлению специфичности и некоторых свойств АТФ-азы сетчатки показали, что при замене в среде инкубации АТФ на АМФ активность фермента в ядрах ганглиозных клеток, кровеносных сосудах и глиальных элементах сетчатки значительно снижается, но полностью не исчезает. [29]
Отмытые и подсушенные кусочком фильтровальной бумаги электроды полярографа ( или рН - метра) осторожно погружают в кювету с 2 мл среды инкубации ( в которую предварительно добавлен 5 - 10 - 6 М ротенон) до полного удаления воздуха из пространства над поверхностью жидкости. Включают самописец и с помощью потенциометра Чувствительность устанавливают максимальное значение тока, соответствующее исходному содержанию кислорода в среде. Убедившись в отсутствии изменений тока во времени ( дрейф), в кювету добавляют около 40 мкл густой суспензии митохондрий ( 4 - 5 мг белка) и через 1 - 2 мин реакцию начинают добавлением 5 - 10 мМ сукцината. Регистрируют окисление сукцината в контролируемом состоянии, происходящее с постоянной скоростью на протяжении 1 - 2 мин. После этого в кювету добавляют 200 мкМ АДФ и регистрируют быстрое окисление сукцината в процессе окислительного фосфорилирования. Спустя некоторое время скорость дыхания замедляется, что связано с переходом митохондрий в контролируемое состояние при исчерпании АДФ. Дыхание регистрируют еще 1 - 2 мин, после чего в кювету добавляют АДФ или 50 мкМ ДНФ для быстрого исчерпания кислорода в среде. Из проведенного опыта убеждаются в высокой степени сопряженности препарата митохондрий и рассчитывают скорость окислительного фосфорилирования и коэффициент АДФ / О. [30]
Страницы: 1 2 3 4