Неводная среда
Cтраница 3
В неводных средах можно титровать как бесцветные, так и-окрашенные растворы. [31]
В неводных средах перегруппировка сильно замедляется. [32]
В неводных средах порядок основности, по-видимому, следующий: кетон сложный эфир кислота, но в настоящее время было бы рискованно предсказывать значения р / Со алифатических сложных эфиров. Однако критерий этот сомнителен, так как он приводит к выводу, чтоцикло-гексанон ( р / Са - - 6 8) [61 ] более основен, чем тетрагидрофуран ( р / С0 - 2 08) [13], вопреки большинству других способов оценки силы оснований. [33]
В неводных средах можно получить содержащие NO соля нитрония: ( NO) HSO4 ( NO) C1O4 и др. ( см. разд. [34]
В неводных средах ток заряжения может быть несколько больше, так что в некоторых растворителях предел обнаружения увеличен. Для кинетических предельных токов предел обнаружения может быть выше или ниже, чем для диффузионного предельного тока, в зависимости от механизма электродного процесса ( см. разд. [35]
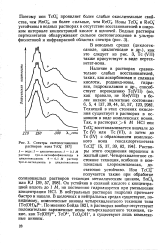 |
Спектры светопрглощения растворов иона TcOJ. [36] |
В неводных средах ( циклогек-саноле, циклогексане и др.), как это следует из рис. 3, Тс ( VII) также присутствует в виде пертех-нетат-иона. [37]
В неводных средах образующийся иодамид осуществляет процесс иодирования. В присутствии воды возможен следущий ход. [38]
В неводных средах, например в смесях метанол - бензол ( 1: 1), в качестве оптимального фона для определения пероксидов рекомендуется 0 3 М LiCl ( Льюис, Квакенбуш и Фриз), в связи с чем этот раствор во многих работах принят в качестве основного фона при полярографическом определении различных пероксидов. [39]
В неводных средах можно получить соли, содержащие катион нитрозила NO: ( NO) HSO4, ( NO) C1O4 и др. ( см. разд. [40]
 |
Зависимость констант диссоциации от температуры. [41] |
В неводных средах соли обычно ведут себя как электролиты средней силы или слабые. [42]
В органических неводных средах могут быть получены комплексные гидриды, в которых часть атомов водорода замещена на другие лиганды. Число таких соединений довольно велико. Их образуют все переходные металлы пятой, шестой, седьмой и восьмой групп. [43]
В неводных средах скорости образования хелатных полимеров могут быть весьма небольшими. [44]
Переход на неводные среды и возврат соли NaCl на электролиз с целью получения хлора и каустика открывает новые возможности для хлорного метода синтеза хлоргидринов и окисей на их основе в хлорной подотрасли химической промышленности. [45]
Страницы: 1 2 3 4