Слабокислая среда
Cтраница 1
Слабокислая среда облегчает образование медноаммиачного комплекса с ацетиленом; высокое содержание НС1 в катализатор-ном растворе влечет за собой увеличение выхода винилхлорида и ацетальдегида и частичный переход образовавшегося винилацети-лена в хлоропрен. Наиболее выгодным является содержание 0 4 вес. Добавка НС1 сверх этой концентрации снижает скорость реакции и выход винилацетилена. [1]
Слабокислая среда при сочетании создается или поддержанием очень небольшой концентрации минеральной кислоты или путем добавления в реакционную массу уксуснокислого натрия. [2]
Из слабокислой среды галлий экстрагируется раствором 8-оксихинолина в хлороформе. [3]
Из слабокислой среды торий экстрагируется раствором НТТА в бензоле. [4]
Из слабокислой среды теллур сорбируется на катионитах, например на К. [5]
В слабокислой среде ( рН 5 - 6 5) из мочевины и формальдегида при избытке формальдегида образуются низкомолекулярные смолы ( олигомеры), молекулярная масса которых определяется температурой и продолжительностью реакции поликонденсации. [6]
В слабокислой среде оксазолиновое кольцо легко разрывается по связи между углеродом и азотом с образованием О-бензоилпроизводного исходной аминокислоты. [7]
В слабокислой среде в качестве водорастворимых перекисных соединений используется перекись водорода [22], а такие ее производные, как пербораты и перкарбонаты, не нашли никакого технического применения. [8]
В слабокислой среде восстановление иодата происходит медленно. При рН 5 скорость восстановления часто падает до нуля, восстановление происходит только при действии очень сильных восстановителей. [9]
В слабокислой среде восстановление иодата происходит медленно. При рН 5 скорость восстановления часто падает до нуля, восстановление происходит только при действии очень сильных восстановителей. [10]
В слабокислой среде ( например, буферный раствор ацетата) происходит Протонирование кислородного атома гидроксильной группы, после чего следуют элиминирование воды и потеря протона группой NH, приводящие к образованию конечного продукта реакции. На первый взгляд может показаться удивительным, что протонирова-ние продукта присоединения осуществляется не по атому азота, а по атому кислорода, хотя хорошо известно, что амины более сильные основания, чем спирты. [11]
В слабокислой среде устойчивость V ( 5) возрастает. [12]
В слабокислой среде устойчивость V ( 5) возрастает. Кроме того, в кислой среде образуются не катионы V4 или V5, а их оксопроизводные - ванадилы. [13]
В слабокислой среде с увеличением содержания в растворе НС1 степень диссоциации аминогрупп повышается. В результате электростатическое отталкивание групп - RNHJ возрастает и происходит развертывание молекулярных клубков полиамфолита. Это сопровождается увеличением вязкости и уменьшением мутности раствора. При значительном содержании НС1 ( большое количество хлорид-ионов) степень диссоциации основных групп понижается в результате образования солевой формы RNH3C1, а эффективные размеры молекулы снова уменьшаются. [14]
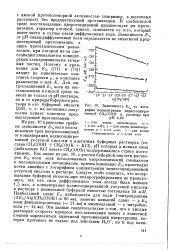 |
Зависимость Е, от лога. [15] |
Страницы: 1 2 3 4