Хлоридная среда
Cтраница 1
Хлоридные среды применяются также для выделения цинка, который хорошо поглощается анионитами из разбавленных ( например, 0 5М) растворов соляной кислоты. При низких концентрациях соляной кислоты кадмий имеет более высокий коэффициент распределения, чем цинк. Для разделения этих элементов сначала элюируют цинк 0.02 М НС1 [69], а затем - кадмий разбавленной азотной кислотой. [1]
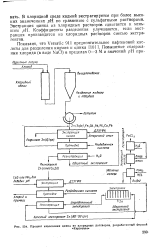 |
Процесс извлечения цинка из хлоридных растворов, разработанный фирмой. [2] |
В хлоридной среде кадмий экстрагируется при более высоких знамечениях рН по сравнению с сульфатными растворами. Коэффициенты разделения улучшаются, если экстракция производится из хлоридных растворов смесью экстра-гентов. [3]
В хлоридных средах величина 6емк уже значительно больше, но полного заполнения поверхности также практически не наблюдается. [4]
Трудности разделения в хлоридных средах, связанные с явлениями гидролиза и полимеризации, легко устраняются добавлением плавиковой кислоты. Плавиковая кислота образует прочные комплексы с теми элементами, которые склонны к гидролизу и полимеризации в хлоридных растворах. [5]
 |
Зависимость тока ( 1 и валентно-сти ( 2 растворения титана от потенциала в деаэрированной 8 н. НС1, 21 С, п - 1000 об / мин. [6] |
Типичные анодные потен-циостатические кривые титана в хлоридных средах с рН от - 0 078 до 2 00 приведены на рис. 2.4. Аналогичные данные имеются и для многих других хлоридных и сульфатных сред. [7]
Исследованы особенности анодного активирования хромистых чугунов в хлоридных средах. Химический состав исследованных чугунов приведен в таблице. [8]
 |
Влияние максимальной растягивающей нагрузки ( при изгибе на КР хромистых сталей и стали 08Х18ШОТ ( для сравнения в насыщенном паре над водой, содержащей 30 г / л NaCl, при 300 С. [9] |
Склонность к КР сталей типа Х13 в высокотемпературных хлоридных средах сильно зависит от их структуры и режима термообработки. После закалки на мартенсит с низким отпуском стойкость низка, она заметно растет при высоком отпуске ( 650 - 780 С), увеличиваясь с повышением температуры отпуска. [10]
Аналогичный механизм установлен для растворения железа в кислых хлоридных средах. [11]
В результате ионного силицирования молибдена циркуляционным методом в безводородной хлоридной среде наблюдается ускорение диффузионного насыщения в 2 - 3 раза по сравнению с силицированием в циркуляционной установке с печным нагревом. При этом получается иная структура покрытия, имеющая более высокую жаростойкость. [12]
Среди анионообменных методов наибольшее значение имеют разделения в хлоридных средах, особенно в солянокислых растворах. Солянокислая среда чрезвычайно удобна как для разделения металлов, принадлежащих к рассматриваемым группам, так и для их отделения от других элементов. Выбрав подходящие условия, можно совершенно избежать перекрывания полос элюирования при разделении рассматриваемых металлов. [13]
Свойства нитратных растворов во многих отношениях сходны со свойствами хлоридных сред. [14]
Легирование молибденом повышает общую коррозионную стойкость аустенитных сталей в хлоридных средах, в том числе заметно возрастает устойчивость против пштинговой коррозии. Однако введение до 2 - 3 % Мо снижает устойчивость сталей с 12 - 40 % Ni против КР в кипящем 42 - 45 % - ном растворе MgCl2 и в хлоридсодержащих. Отрицательное влияние отмечается уже при незначительном, примесном количестве, молибдена. [15]
Страницы: 1 2 3 4 5