Сродство - гемоглобин
Cтраница 2
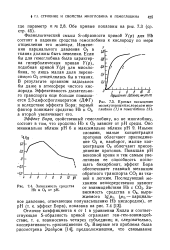 |
Кривые насыщения молекулярным кислородом мио-глобииа ( 1 и гемоглобина ( 2.| Зависимость сродства НЬ к О2 от рН. [16] |
Физиологический смысл S-образности кривой Y ( p) для НЬ состоит в падении сродства гемоглобина к кислороду по мере отщепления его молекул. Изменения парциального давления О2 в тканях должны быть невелики. Если бы для гемоглобина была характерна гиперболическая кривая Y ( p), подобная кривой Y ( p) для миогло-бина, то лишь малая доля переносимого О2 отщеплялась бы в тканях. [17]
 |
Уравнение, суммирующее эффект Бора. НЬ - гемоглобин. [18] |
Органические фосфаты, особенно 2 3-дифосфоглицерат ( ДФГ), также оказывают влияние на сродство гемоглобина к кислороду. [19]
Благодаря этому обеспечивается поступление кислорода из материнской крови в кровь плода, в) ДФГ уменьшает сродство гемоглобина к кислороду. [20]
Соединение двуокиси углерода с гемоглобином имеет большое значение в физико-химическом равновесии крови, поскольку в присутствии углекислоты сродство гемоглобина к кислороду снижается - явление, хорошо известное в физиологии. [21]
И наоборот, в легочных капиллярах выделение СО2 и сопутствующее ему повышение рН крови приводит к увеличению сродства гемоглобина к кислороду. Это влияние величины рН и концентрации СО2 на связывание и освобождение кислорода гемоглобином называют эффектом Бора в честь датского физиолога Христиана Бора, впервые открывшего этот эффект. [23]
Высокая метаболическая активность приводит также к повышению температуры в данном участке тела, а это ведет к уменьшению сродства гемоглобина к О2 и усиленной диссоциации оксиге-моглобина. В результате кривая диссоциации тоже сдвигается вправо, и это имеет физиологический смысл, так как в активные участки поступает больше кислорода из крови. [24]
Уже давно известно, что 23-дифосфоглицерат ( рис. 1) присутствует в эритроцитах в довольно высоких концентрациях, однако функция этого соединения оставалась загадкой до тех пор, пока не было обнаружено, что он оказывает сильное влияние на сродство гемоглобина к кислороду. [26]
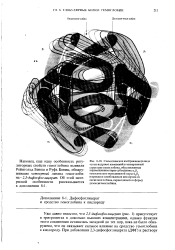
Важной особенностью гемоглобина, которая обусловлена наличием нескольких гем-групп, является форма кривой связывания кислорода: не простая гипер болическая кривая насыщения, как для миоглобина, а S-образная. Сродство гемоглобина к кислороду возрастает с давлением. Поэтому при умеренных давлениях гемоглобин эффективно связывает кислород в легких, но отдает его мио-глобину при низких давлениях в тканях. При потере кислорода образуется дезоксигемоглобин, субъединицы молекулы слегка смещаются относительно друг друга - и поворачиваются так, что два р-гема удаляются друг от друга на расстояние около 6 5 А. Эта конформационная перестройка, несомненно, тесно связана с кооперативным взаимодействием гемов, которое позволяет им более прочно связывать кислород, когда молекула уже частично окислена. Однако детали этого взаимодействия еще не ясны. [27]
Когда вдыхаемый воздух содержит окись углерода, происходит конкуренция между О2 и СО за одно и то же количество гемоглобина. Если бы сродство гемоглобина к СО было так же велико, как и сродство к О2, а вдыхаемый воздух содержал равные концентрации О2 и СО, то равновесие установилось бы, когда половина гемоглобина превратилась в НЬО2, а половина - в НЬСО. [28]
Они также угнетают активность некоторых ферментов, участвующих в гликолизе эритроцитов, и снижают содержание 2 3 - дифосфоглицерата красных кровяных клеток. В результате увеличивается сродство гемоглобина и кислорода, что может уменьшить поступление кислорода к тканям. [29]
Из этих данных ясно, что сродство гемоглобина к кислороду определяется не только его простетической группой и глобином, но и какими-то факторами, присутствующими в красных кровяных тельцах. [30]
Страницы: 1 2 3 4