Сродство - гемоглобин
Cтраница 3
Реут и Ардавичене в опытах на крысах показали, что уменьшение числа эритроцитов при таллотоксикозе сопровождается снижением их кислотной резистентности и увеличением максимума распада эритроцитов. При этом в них нарастает уровень 2 3-дифос-фоглицериновой кислоты, снижающей сродство гемоглобина к кислороду. [31]
Способность гемоглобина связывать кислород зависит от ряда факторов. В тканях, где значение рН несколько меньшее по сравнению с легкими, а концентрация С02 достаточно высока, сродство гемоглобина к кислороду снижается, кислород отделяется, а С02 и протон водорода присоединяются к гемоглобину. Этот феномен называется эффектом Бора в честь ученого, впервые открывшего это явление. В реализации данного эффекта кроме гемоглобина и кислорода участвуют С02 и протон водорода. Дезоксигемоглобин представляет собой прото-нированную форму пигмента. [33]
Регулирующее влияние ДФГ на сродство гемоглобина к кислороду в эритроцитах зависит от величины парциального давления кислорода в легких. После того как здоровый человек поднимется, скажем, на высоту 4000 м над уровнем моря, в течение первых нескольких часов концентрация ДФГ в его эритроцитах будет возрастать; при этом число молекул ДФГ, связанных с гемоглобином, увеличится, а сродство гемоглобина к кислороду снизится. На большой высоте парциальное давление кислорода значительно ниже, чем на уровне моря. Поэтому и в тканях парциальное давление кислорода снижается. Увеличение содержания ДФГ в эритроцитах при восхождении на большую высоту облегчает освобождение кислорода из гемоглобина в тканях. Изменения противоположного характера наблюдаются у людей, акклиматизировавшихся к условиям высокогорья, например у жителей Гималаев или Андов, когда они спускаются в долины. [34]
Однако у гемоглобина А сродство к кислороду при этом становится выше, чем у гемоглобина F. Если в препараты гемоглобина вновь добавить ДФГ, то кривые насыщения кислородом примут прежний вид, показанный на рисунке. Какое влияние оказывает ДФГ на сродство гемоглобина к кислороду. [35]
Кислородная емкость крови может быть повышена путем увеличения числа циркулирующих эритроцитов при акклима-ции к теплу. Наряду с этим возможно также изменение регу-ляторной функции гемоглобина. Например, у сомика Ictalurus nebulosus при тепловой акклимации повышается сродство гемоглобина к кислороду. Молекулярной основой этого эффекта, по-видимому, служит какое-то изменение в составе ци-интактных эритроцитов. Когда гемоглобины рыб, акклимирован-ных к теплу и к холоду, выявляются только при исследовании интактных эритроцитов. Когда эритроциты рыб, акклимирован-ных к теплу и холоду, изолировали из нормальной для них внутриклеточной среды и получали кривые насыщения для растворов свободного НЬ, то никакой разницы в значениях Р5о обнаружено не было. Дополнительные данные в пользу того, что функциональные различия между гемоглобинами рыб, ак-климированных к теплу и к холоду, зависят от изменений среды, в которой функционирует пигмент, были получены при изучении электрофореграмм гемоглобина: в обоих случаях здесь оказалось 7 зон гемоглобина, и относительные количества соответствующих компонентов были примерно одинаковыми при акклимации того и другого типа. Таким образом, весьма вероятно, что сезонная адаптация системы транспорта О2 у некоторых эктотермных видов может быть сходна по своим механизмам с адаптацией к большим высотам у человека: общая емкость этой системы регулируется путем изменений в количестве циркулирующего гемоглобина, в то время как способность НЬ присоединять и отдавать кислород адаптивно модулируется путем изменений в цитозоле эритроцитов. [36]
Животные, обитающие в условиях некоторого недостатка и пониженного парциального давления кислорода, обладают определенными адоптациями. Показано, что млекопитающие, обитающие в подземных убежищах, легче переносят некоторый избыток СОг ( гиперкапния) и недостаток Оз, чем виды, не суживающиеся с такими условиями в природе. Адаптивные механизмы в первую очередь связаны с улучшением дыхательных свойств крови, в частности с увеличением сродства гемоглобина к кислороду. [37]
Кривая насыщения гемоглобина кислородом имеет сиг-моидную форму, поэтому гемоглобин хорошо приспособлен для связывания кислорода в легких и его освобождения в периферических тканях. Миоглобин в отличие от гемоглобина обладает значительно более высоким сродством к кислороду и характеризуется гиперболической кривой насыщения кислородом, благодаря чему он наделен способностью запасать кислород в мышцах. Эти соотношения, равно как и регулирующее воздействие связывающегося с гемоглобином 2 3-дифосфоглицерата ( ДФГ) на сродство гемоглобина к кислороду, обусловлены наличием у гемоглобина четырех специфических центров связывания с О2, СО2, ионами Н и ДФГ, а также изменениями в четвертичной структуре гемоглобина в цикле оксигенация-де-зоксигенация. Таким образом, субъединицы гемоглобина, подобно субъединицам других олигомерных белков, способны передавать сигналы о регуля-торных взаимодействиях посредством конформационных изменений молекулы белка. Изменения в аминокислотной последовательности глобулярных белков, обусловленные генными мутациями, например замена двух аминокислотных остатков в молекуле гемоглобина при серповидноклеточной анемии, могут вызвать значительные изменения конфор-мации белка и, следовательно, сказаться на его биологических функциях. [38]
Высокие концентрации оксида углерода могут привести к физиологическим и патологическим изменениям и неожиданной смерти человека. Оксид углерода можно считать вдыхаемым ядом, который лишает ткани тела необходимого им кислорода. Оксид углерода, соединяясь с гемоглобином крови, образует карбоксигемоглобин СО-Нв, соединение же кислорода с гемоглобином дает оксигемог-лобин О2 - Нв, Сродство гемоглобина с СО примерно в 210 раз выше его сродства с кислородом. Процесс образования в крови карбокси-гемоглобина - обратимый. Когда вдыхание оксида углерода прекращается, СО, связанный с гемоглобином, постепенно выделяется, и кровь человека очищается от оксида углерода наполовину за каждые 3 - 4 часа. Прямое воздействие карбоксигемоглобина состоит в уменьшении способности крови переносить кислород, кроме того. СО-Нв мешает реализации кислорода, переносимого остальным гемоглобином, что еще больше уменьшает способность крови к переносу кислорода. Оксид углерода не имеет запаха и вкуса, что делает его особенно опасным. [39]
Высокие концентрации оксида углерода могут привести к физиологическим и патологическим изменениям и неожиданной смерти человека. Оксид углерода можно считать вдыхаемым ядом, который лишает ткани тела необходимого им кислорода. Оксид углерода, соединяясь с гемоглобином, образует карбоксигемог-лобин СО-Нв, соединение же кислорода с гемоглобином дает ок-сигемоглобин 02 - Нв. Сродство гемоглобина с СО примерно в 210 раз выше его сродства с кислородом. Процесс образования в крови СО-Нв - обратимый. Когда вдыхание оксида углерода прекращается, СО, связанный с гемоглобином, постепенно выделяется, и кровь человека очищается от оксида углерода наполовину за каждые 3 - 4 час. Прямое воздействие карбоксигемоглобина состоит в уменьшении способности крови переносить кислород, кроме того СО-Нв мешает реализации кислорода, переносимого остальным гемоглобином, что еще больше уменьшает способность крови к переносу кислорода. Оксид углерода не имеет запаха и вкуса, что делает его особенно опасным. [40]
Оксид углерода СО - бесцветный газ без запаха и вкуса - не оказывает, по-видимому, никакого воздействия на поверхности материалов, на жизнедеятельность высших растений. Однако многочисленные исследования показали, что высокие концентрации его могут привести к физиологическим и патологическим изменениям и даже к неожиданной смерти. Оксид углерода можно считать вдыхаемым ядом, который лишает ткани тела необходимого им кислорода. Сродство гемоглобина с СО примерно в 210 раз выше ei) 0 сродства с кислородом. К счастью, процесс образования в крови СОНЬ - обратимый. Когда вдыхание оксида углерода прекращается, СО, связанный с гемоглобином, постепенно выделяется, и кровь человека уже через 3 - 4 часа наполовину очищается от оксида углерода. Прямое воздействие карбоксигемоглобина состоит в уменьшении способности крови переносить кислород и к тому же мешает реализации кислорода, переносимого остальным гемоглобином. [41]
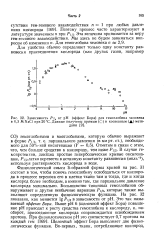 |
Зависимость Р /, от рН ( эффект Бора для гемоглобина человека в 0 3 М NaCl при 20 СС. Данные получены прямым ( С и косвенным ( методами. [42] |
Физиологический смысл S-образной формы кривой на рис. 31 состоит в том, чтобы помочь гемоглобину освободиться от кислорода в процессе переноса его в клетки ткани там и тогда, где и когда кислород более необходим, а именно там, где парциальное давление кислорода минимально. Большинство типичных гемоглобинов обнаруживает и другие необычные вариации Р, которые также выполняют определенную физиологическую функцию. Выше рН 6 ( щелочной эффект Бора) повышение рН приводит к росту сродства гемоглобина к кислороду, и, наоборот, присоединение кислорода сопровождается освобождением протона. Щелочный эффект Бора выполняет две физиологические функции. [43]
 |
Влияние ДФГ на кривую насыщения гемоглобина кислородом. [44] |
При обычном выделении гемоглобина из крови он содержит довольно большое количество ДФГ, от которого трудно освободиться полностью. При полном удалении ДФГ из гемоглобина кривая связывания его с кислородом в значительной степени утрачивает свою сигмоидную форму и гемоглобин приобретает намного более высокое сродство к кислороду. В эритроцитах некоторых птиц содержится не ДФГ, а другое фосфатсодержащее со-едикепие-инозитолгексафосфат, который даже еще более эффективно, чем ДФГ, снижает сродство гемоглобина к кислороду. [45]
Страницы: 1 2 3 4
