Стабильность - катион
Cтраница 1
Стабильность катиона определяется изменением свободной энергии при его образовании. Данные по термодинамике соответствующих реакций ограничены; известны гл. [1]
Относительно стабильности катионов см. разд. [2]
Естественно, если стабильность катиона достаточно низка, взаимодействие нуклеофила с субстратом может осуществляться в ионной паре, и стереохимия реакции будет меняться. [3]
 |
Факторы парциальных скоростей реакции нротодетритирования фторзаме-щенных бнфенилов АгС Н4Т. [4] |
Примерно такое же уменьшение стабильности трифенилметиль-ного катиона происходит при введении К02 - грушш в пара-положение бензольного кольца. Значение рКв для ( С6Р6) 3СОН вычисленное по аддитивной схеме с учетом данных, приведенных в табл. 21, составляет - 18 1, что достаточно хорошо соответствует экспериментальному значению. [5]
Влияние различного характера заместителей на стабильность катионов и радикалов проявляется в целом таким же образом, как и в реакциях, протекающих в растворах. [6]
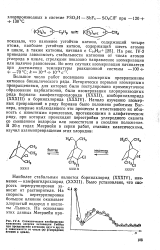 |
Схематическое изображение изменения энергии активации Гиббса при превращении катионов друг в друга в зависимости от числа ( п углеродных атомов в цикле. [7] |
На рис. IV-2 приведена зависимость стабильности катионов от числа атомов углерода в цикле, стрелками показано направление изомеризации или наличие равновесия. [8]
Для оценки влияния заместителей на изменение стабильности катионов можно использовать различие энергий Гиббса указанного процесса для соответственно разных соединений RX и R X: значение ДАО0 катионов количественно характеризуют изменение стабильности катионов при смене заместителей. Относительная термодинамическая стабильность катионов, которая отражает в основном электронные эффекты заместителей, может быть установлена только при определении / Ср с одним и тем же X ( уходящей группой) в одном и том же растворителе. При определении AG указанным методом пренебрегают AAG0 исходных соединений, которое обычно большого значения не имеет. [9]
Из этих двух работ следует, что увеличение стабильности исходного катиона приводит к увеличению порядка связи с нуклео-филом, что согласуется с постулатом Хэммонда. [10]
В последних примерах электронодонорные метальные группы способствуют рассредоточению положительного заряда и этим повышают стабильность катиона. При образовании карбаниона они, как более электронодонорные, чем атомы водорода, способствуют фиксации неподеленной пары электронов на одном атоме углерода и снижают стабильность карбаниона, а следовательно, уменьшают вероятность его образования. На этом основании первичные карбанионы должны быть более устойчивыми, чем вторичные, и тем более третичные. [11]
Для оценки влияния заместителей на изменение стабильности катионов можно использовать различие энергий Гиббса указанного процесса для соответственно разных соединений RX и R X: значение ДАО0 катионов количественно характеризуют изменение стабильности катионов при смене заместителей. Относительная термодинамическая стабильность катионов, которая отражает в основном электронные эффекты заместителей, может быть установлена только при определении / Ср с одним и тем же X ( уходящей группой) в одном и том же растворителе. При определении AG указанным методом пренебрегают AAG0 исходных соединений, которое обычно большого значения не имеет. [12]
Алкилыше катионы, генерируемые при взаимодействии ал-килирующего реагента и катализатора или при отщеплении от аренониевого иона, претерпевают типичную для карбокатио-нов скелетную сигматропную перегруппировку с образованием более термодинамически стабильного карбокатиона. Стабильность катионов уменьшается в ряду: третичный вторичный; первичный, поэтому часто оказывается, что, вступившие в ароматическое кольцо алкильные группы изомерны алкильным группам, содержавшимся в реагенте. Например, при алкшшро-вании w - пропилбромидом образуются преимущественно изо-пропилзамещенные. Изомеризация может происходить как до, так и после реакции алкилирования. [13]
Согласно представлениям Перли [16], катионный обмен зависит частично от размера иона, числа кислородов-соседей, связанных со щелочным или щелочноземельным ионом, электростатических сил, превалирующих внутри стеклянной структуры, и способности щелочных ионов взаимодействовать с водой. Стабильность катионов внутри решетки качественно объясняется правилами координационной химии, хотя связи здесь, конечно, не ковалентны. Ион калия с координационным числом десять, чтобы достичь определенной стабильности, должен ассоциироваться с большим количеством кислорода, чем меньший по размеру ион натрия с координационным числом шесть. Тем не менее, расстояние между центрами атомов кислорода и большого иона калия обязательно должно быть больше, чем для небольшого иона натрия и связь будет соответственно слабее. Двухвалентные катионы образуют с кислородом более сильные связи, чем одновалентные. [14]
Стабильность катиона определяется суммой тех же факторов, что и стабильность аниона, с той лишь разницей, что влияние этих факторов на основность противоположно тому влиянию, которое они оказывали на кислотность. [15]
Страницы: 1 2 3