Стабильность - комплекс
Cтраница 2
Стабильность комплексов определяется не только основностью лигандов, она зависит также от образования хелатных узлов и других элементов пространственной структуры у би-и полидентатных лигандов. В зависимости от - структуры лиган-да хелатные кольца могут быть плоскими или иметь гош-кои-фигурацию, причем комплексы с недеформированными кольцами более стабильны. Устойчивость также зависит от величины центрального иона, но обычно наиболее стабильны комплексы, содержащие пяти - и шестичленные циклы. Для колец величиной 4 или 7 устойчивость снижается. [16]
Стабильность комплекса определяется силой кислот и оснований Льюиса ( гл. [17]
Стабильность комплексов возрастает с удлинением цепи нормального алкана. Это объясняется тем, что между молекулами углеводородов, находящимися в канале, сохраняется расстояние 0 24 нм. Чем короче молекулы нормальных алканов, тем больше доля пустот - незаполненных участков в канале - и тем менее энергетически выгодно образование карбамндпых комплексов, протекающее с выделением тепла. Например, теплота комплексооб-разования при переходе от гексадекана к октану уменьшается от 88 до 33 1 кДж / моль. Образование аддуктов с гексаном и еще более низкокипящнми нормальными алканами энергетически невыгодно, и при комнатной температуре и атмосферном давлении выделить соответствующие комплексы не удается. [18]
Стабильность комплексов растет с увеличением числа ме-тильных групп в м - и п-положениях колец, и она выше, чем у незамещенного бифенила. Орто-метильные группы снижают устойчивость комплексов: уже в монометнльном она ниже, чем у бифенила, и резко падает по мере выхода ядер из пла-нарности при дальнейшем замещении четырех о-положенин. Это подтверждается и данными по системам, сходным с бифенилом - фенилнафталинам. [19]
Стабильность комплексов полиалкилбензолов с монохлористым иодом состава 1: 1 тоже несколько изменяется в зависимости от структуры алкильных заместителей, а также от положения заместителей относительно друг друга в ароматическом ядре. Как видно из данных рис. 14, изменения этого рода обычно невелики. [20]
Стабильность комплексов иода с первичными аминами ( RNH2) в зависимости от R изменяется в следующем порядке: н-бутилэтилметил; для третичных аминов ( RsN) изменение стабильности имеет противоположный ход. Это приписывают неблагоприятному стерическому влиянию объемистых заместителей ( R) на донорную силу третичного амина. [21]
Стабильность комплексов металлов, в свою очередь, связана с таким свойством, как потенциал ионизации. Такая же связь имеется между стабильностью и электроотрицательностью. [22]
Стабильность комплексов состава 1: 2 увеличивается в ряду бензол - толуол-ж-ксилол - мезитилен, а стабильность комплексов состава 1: 1 - при переходе от ж-ксилола к мезитилену. Для комплексов состава 1: 2 зависимость между AG и потенциалами ионизации ароматических углеводородов линейна. [23]
Стабильность комплексов иона серебра увеличивается по мере перехода от бензола к толуолу и далее к ксилолам. Для комплексов полиэтилбензол - ион серебра отмечен аналогичный ход изменения стабильности, которая в общем несколько меньше, чем для аддуктов соответствующих полиметилбензолов. Считают, что относительно низкая устойчивость комплексов полиалкил-бензолов вызывается, по крайней мере частично, неблагоприятными стерическими взаимодействиями между алкильными группами и молекулами растворителя, которые ассоциированы с ионом серебра, находящимся в комплексе. В связи с этим интересно отметить, что три-грег-бутилбензол образует значительно менее стабильный аддукт с ионом серебра, чем 1, 3 5-триэтил-бензол, в то время как комплексы этилбензола и трег-бутилбен-зола обладают сравнимой стабильностью. [24]
Стабильность комплекса ионного типа определяется зарядом и радиусом центрального иона. Стабильность же комплекса ко-валентного типа характеризуется ионизационным потенциалом центрального иона. [25]
Стабильность комплекса ионного типа определяется зарядом и радиусом центрального иона. Стабильность же комплекса ко-валентного типа характеризуется ионизационным потенциалом центрального иояа. [26]
Поэтому стабильность комплекса будет выше, если эта орбиталъ не занята. Но на восьми орбиталях Xi - % 8 могут разместиться лишь 16 электронов. Четыре лиганда имеют восемь электронов, участвующих в образовании связей М - Ьф Следовательно, плоские квадратные комплексы ML. [27]
На стабильность комплексов оказывает влияние и природа донорного атома лигандов. В случае жестких центр, атомов уменьшение размера донорного атома лиганда и повышение его электронной плотности приводит к увеличению стабильности комплексов, что находится в соответствии с усилением координац. [28]
На стабильность комплекса значительно влияет температура. Комплекс, образующийся на активном центре, очень легко разлагается при 150; при этом выделяется молекула сильного основания ( КОН), создающая снова активные центры. [29]
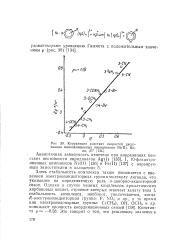 |
Корреляция констант скоростей диссоциации монозамешенных пиридинатов NiСИ. Вода, 25. [30] |
Страницы: 1 2 3 4