Стабильность - комплекс
Cтраница 3
Здесь стабильность комплекса также понижается с введением электроноакцепторных групп в молекулу лиганда, что указывает на определяющую роль ст-донорно-акцепторной связи. [31]
Уменьшение стабильности комплекса металла в присутствии недостаточного количества лиганда или при использовании лиганда, с которым металл образует малопрочный комплекс. [32]
Уменьшение стабильности комплекса металла в присутствии недостаточного количества лиганда или при использовании ли-ганда, с которым металл образует малопрочный комплекс. [33]
Это соответствует стабильности комплексов с пятью и шестью координационными местами, прочных в условиях водных растворов. Далее было найдено, что коэффициент задержки пропорционален в случае вторичных и третичных аминов константе диссоциации аминов, в то время как в случае первичных аминов и пиридиновых производных намечается зависимость от способности образовывать водородные связи или от стерического эффекта. [34]
Так как стабильность комплекса зависит от стереохимических факторов, это различие находится в соответствии с утверждением, что природа межнуклеотидной связи ( 2 - 5 - или 3 - 5) влияет на расстояния между плоскостями или на другие структурные факторы. [35]
Это соответствует стабильности комплексов с пятью и шестью координационными местами, прочных в условиях водных растворов. Далее было найдено, что коэффициент задержки пропорционален в случае вторичных и третичных аминов константе диссоциации аминов, в то время как в случае первичных аминов и пиридиновых производных намечается зависимость от способности образовывать водородные связи или от стерического эффекта. [36]
Действительно, стабильность комплексов циклобута-диеновых производных с металлами породила теперь другую проблему, касающуюся их собственной стабильности. [37]
Связана со стабильностью комплексов и электроотрицательность, которая является мерой. Этим может быть объяснена корреляция токсичности с алектроотрицательностью. Но электроотрицательность и потенциал ионизации в свою очередь связаны с положением элемента в периодической системе, со строением электронной оболочки. Так, первичный потенциал ионизации уменьшается по мере увеличения атомного номера элемента в своей группе. В силу этого при расчете корреляции токсических доз металлов с этими двумя показателями в одном случае получена прямая, а в другом обратная связь. [38]
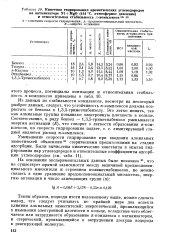 |
Кинетика гидрирования ароматических углеводородов. [39] |
Из данных по стабильности комплексов, несмотря на некоторый разброс данных, следует, что устойчивость л-комплексов должна возрастать от бензола к 1 3 5-триметилбензолу. Это легко понять, так как алкильные группы повышают электронную плотность в кольце. [40]
Таким образом, стабильность комплекса в большей степени зависит от его стереохимии. Если же в координационной сфере присутствуют два или более хиральных лиганда, их взаимодействие ( непосредственное или через молекулы растворителя в первой или второй координационной сфере) может привести к различию в стабильности комплексов и, следовательно, к энантиоселективности. [41]
Известно, что стабильность комплекса часто можно увеличить введением дополнительных ароматических колец [14]; при этом возрастает и интенсивность окрашенного комплекса. Необходимо отметить, что, хотя интенсивно окрашенные комплексы всегда довольно стабильны, обратное не всегда верно. Например, цианид или этилендиаминтетрауксусная кислота ( ЭДТК) являются бесцветными ком-плексообразующими агентами, но тем не менее они образуют стабильные комплексы. Присутствие резонирующих структур благоприятно для окрашивания. [42]
Если рН 10 стабильность комплекса уменьшается, а конечная точка делается нечеткой. [43]
Ацетат аммония способствует стабильности комплексов. [44]
 |
Кинетика гидрирования ароматических углеводородов. [45] |
Страницы: 1 2 3 4